- CoCl2
-
Kristallstruktur 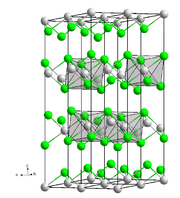
__ Co2+ __ Cl- Allgemeines Name Cobalt(II)-chlorid Andere Namen Cobaltdichlorid
Verhältnisformel CoCl2 CAS-Nummer 7646-79-9 (wasserfrei)
7791-13-1 (Hexahydrat)Kurzbeschreibung blauer kristalliner Feststoff (wasserfrei) [1] Eigenschaften Molare Masse 129,84 g·mol−1 (wasserfrei) Aggregatzustand fest
Dichte 3,356 g·cm−3 [1]
Schmelzpunkt 735 °C [1]
Siedepunkt 1049 °C [1]
Löslichkeit leicht löslich in Wasser: 529 g·l−1 (20 °C)[1] und Alkohol
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 

Giftig Umwelt-
gefährlich(T) (N) R- und S-Sätze R: 49-60-22-42/43-68-50/53 S: 53-45-60-61 MAK nicht festgelegt, da krebserregend[1]
WGK 3 – stark wassergefährdend[1] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Cobalt(II)-clorid ist eine chemische Verbindung von Cobalt und Chlor. Es ist ein im wasserfreien Zustand blaues, als Hexahydrat rosafarbenes Salz.
Inhaltsverzeichnis
Gewinnung und Darstellung
Cobalt(II)-chlorid lässt sich aus den Elementen oder durch Erhitzen des Hexahydrates gewinnen. Letzteres kann wiederum durch Reaktion von Cobalt(II)-hydroxid oder Cobalt(II)-carbonat mit Salzsäure gewonnen werden.
Eigenschaften
Wasserfreies Cobalt(II)-chlorid ist sehr hygroskopisch und nimmt leicht Wasser auf. Dabei ändert es sehr charakteristisch seine Farbe von blau nach rosa. Der entgegengesetzte Farbwechsel von rosa auf blau ist ebenfalls möglich, indem man das Hexahydrat auf Temperaturen oberhalb 35 °C erhitzt. [3]
Verwendung
Wegen des typischen Farbwechsels dient es als Feuchtigkeits-Indikator in Trockenmitteln wie etwa Silica-Gel. Mit Hilfe von Cobalt(II)-chlorid lässt sich Wasser auch in anderen Lösungen nachweisen.
Auch wird es als so genannte Geheimtinte benutzt, da es als Hexahydrat in wässriger Lösung auf dem Papier kaum sichtbar ist, wenn es aber erhitzt wird (z. B. über einer Kerze), tritt tiefblaue Schrift hervor.
Sicherheitshinweise
Cobalt(II)-chlorid gilt als krebserzeugend sowie fruchtschädigend und ist möglicherweise erbgutverändernd.
Quellen
- ↑ a b c d e f g Eintrag zu Cobalt(II)-chlorid in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 9.10.2007 (JavaScript erforderlich)
- ↑ Eintrag zu CAS-Nr. 7646-79-9 im European chemical Substances Information System ESIS
- ↑ Holleman-Wiberg: Lehrbuch der Anorganischen Chemie, 102. Auflage, Berlin 2007 S. 1685. ISBN 978-3-11-017770-1.
Wikimedia Foundation.

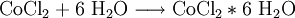
_chloride.jpg)
-chlorid.JPG)