- Erdkeime
-
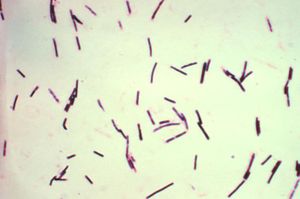
C. perfringens Systematik Abteilung: Firmicutes Klasse: Clostridia Ordnung: Clostridiales Familie: Clostridiaceae Gattung: Clostridium Art: C. perfringens Wissenschaftlicher Name Clostridium perfringens (Veillon & Zuber 1898) Hauduroy et al. 1937 Clostridium perfringens (lat. perfringere = durchbrechen) ist ein stäbchenförmiges, grampositives, endosporenbildendes, unbegeißeltes Bakterium der Gattung Clostridium. In (älterer) Fachliteratur findet sich auch gelegentlich die Bezeichnung „Welch-Fraenkelscher Gasbazillus“[1] bzw. Clostridium welchii[2].
Inhaltsverzeichnis
Vorkommen
C. perfringens ist ein strikter Anaerobier, der das kurzzeitige Aussetzen in sauerstoffreicher Atmosphäre aber problemlos überlebt. Der Organismus kann im Boden (anaerobe Zonen), in Wasser, Staub und Lebensmitteln, aber auch im Darm von Mensch und Tier nachgewiesen werden (1.000 bis 10.000 Keime/g Fäzes). Im Boden zählen Clostridien zu den wichtigsten anaerob Cellulose-abbauenden Mikroorganismen.
Das Temperaturoptimum von C. perfringens liegt bei ca. 43 bis 47 °C (mit Generationszeiten von 8 bis 12 min), Extrembereich min. bei 10 bis 18 °C und max. bei 50 bis 52 °C. Die Sporen können in Abhängigkeit von diversen Umweltfaktoren, Temperaturen von 60 °C überleben. Die Hitzeresistenz ist je nach Stamm sehr variabel und kann bei 100 °C bis zu 60 min betragen. Das Toxin ist hitzelabil (4 min bei 60 °C). Als D-Wert werden 15 bis 145 min bei 90 °C und 0,31 bis 38 min bei 100 °C angegeben.
Toxine
C. perfringens der Serotypen A, B, C, D und E bildet für den Menschen pathogene Exotoxine (Enterotoxine) aus. Durch den Nachweis der wesentlichen Toxine α, β, ε, ι können diese Serotypen des C. perfringens unterschieden werden.[1] Gasbrandbazillen bilden mindestens zwölf Toxine, die als Enzyme (Proteasen, Kollagenasen, Desoxyribonukleasen und Phospholipasen) wirken. Diese Enzyme bauen Gewebe ab und führen zu Nekrosen im betroffenen Muskelgewebe.
Pathogenese und Pathologie
Der Erreger zählt mit weiteren Clostridien zur Gruppe der Gasbrandbazillen und ist der häufigste Erreger des Gasbrands (70 bis 80 %). Darüber hinaus ist das Bakterium häufiger Verursacher der nekrotisierenden Pneumonie, der gangränösen Cholezystitis, einer Sepsis oder anderer unspezifischer Infektionen. In der Humanmedizin sind insbesondere Typ A und Typ C von Bedeutung.[3] Darüber hinaus kann Clostridium perfringens Infektionen des Zentralen Nervensystems verursachen, wovon die häufigste die clostridiale Meningitis ist, die sich meist aus einer Clostridien-Sepsis entwickelt, aber auch infolge von lokalen Traumen oder Operationen, wie der Ausräumung eines subduralen Hämatoms, entstehen kann. Seltener wurden auch Fälle einer clostridialen Enzephalitis beschrieben.[4] Bei Tieren werden die Erkrankungen durch Clostridium-perfringens-Toxine als Enterotoxämie bezeichnet.
Gasbrand
Der durch Clostridium perfringens verursachte Gasbrand gilt als schwerste Form der Wundinfektion und wird auch als „Clostridien-Myositis“, „clostridiale Myonekrose“[1] oder Gasgangrän[5] bezeichnet. Die Infektion entwickelt sich meist nach Verletzungen bei Gartenarbeit oder Tätigkeiten im landwirtschaftlichen Bereich, aber auch nach Bissverletzungen oder Amputationen und hat eine Inkubationszeit von ca. 2 Tagen. Das Infektionsgebiet kennzeichnet sich durch Schwellung und bräunlich-livide Verfärbung. Bei der Palpation kann gegebenenfalls ein „Knistern“ (Crepitatio) festgestellt werden. Aus der infizierten Wunde entleert sich häufig stinkendes, seröses Wundsekret. Erfolgt keine schnelle Behandlung, kann es durch einen toxininduzierten Schock binnen Stunden zum Tod des Infizierten kommen.[1] Trotz optimaler Therapie ist die Letalität hoch und liegt bei 40 bis 60 %. Allerdings ist die Krankheit aufgrund einer guten chirurgischen Versorgung in der Bundesrepublik Deutschland selten geworden; im Jahre 1998 gab es in Deutschland 114 gemeldete Fälle von Gasbrand.[6]
Als pathomechanische Ursache des Gasbrandes lassen sich Clostridium-perfringens-Bakterien vom Serotyp A nachweisen. Diese zerstören durch ihr α-Toxin - eine Lecithinase, die membranständiges Lecithin in Phosphorylcholin und Diacylglycerol spaltet - die Zellmembranen im Infektionsgebiet. Die Vermehrung der toxinbildenden Erreger bzw. die Auskeimung der Sporen von C. perfringens wird dabei durch eine Senkung des Redoxpotentials im Gewebe - beispielsweise bei verminderter Durchblutung, Sekretansammlung oder Nekrose - angeregt. Demzufolge begünstigen Quetschwunden, verschmutzte Schürfwunden, große Wundhöhlen nach Amputation oder Pfählungswunden eine Infektion.[1]
Intestinale Infektionen
C. perfringens zählt zudem zu den Lebensmittelvergiftern. Die Infektionsdosis liegt bei 700.000 Keimen/g, bei Lebensmitteln meist noch höher. Gefährdete Lebensmittel sind warmgehaltenes Fleisch (Rindfleisch, Geflügel), Austern und andere Meeresfrüchte. Die intestinalen Toxininfektionen werden im überwiegenden Teil der Fälle von C.-perfringens-Stämmen vom Typ A verursacht.[1] In den Vereinigten Staaten von Amerika ist Clostridium perfringens mit geschätzten 248.000 jährlichen Fällen die häufigste gemeldete Ursache von Nahrungsmittelvergiftungen. Die nach dem Verzehr auskeimenden Clostridien beginnen im Darm mit der Herstellung des Perfringens-Enterotoxins, das die Durchlässigkeit des Darmepithels steigert und so zu Durchfällen und Darmkrämpfen führt, jedoch selten von Fieber oder Erbrechen begleitet wird. Die ersten Symptome treten innerhalb von 7 bis 15 Stunden nach dem Verzehr der kontaminierten Lebensmittel auf und verschwinden häufig nach 24 Stunden. Die Letalität ist gering.[5]
Wesentlich schwerwiegender ist beim Menschen die durch C. perfringens ausgelöste Enteritis necroticans („Darmbrand“), welche eine hochgradig nekrotisierende Infektion des Jejunums darstellt. Diese wird durch β-toxinbildende Stämme des Bakteriums vom Serotyp C hervorgerufen und verläuft häufig tödlich. Die genauen Pathomechanismen sind noch nicht abschließend geklärt.[1] Im Tierreich verursacht der Typ C die nekrotisierenden Darmentzündung der Saugferkel bzw. die nekrotische Enteritis bei Lämmern, Schafen und Kälbern.[2].
Diagnose
Die Nahrungsmittelvergiftung mittels Clostridium perfringens vom Typ A wird durch Isolierung des Erregers aus dem Darm oder am zuverlässigsten durch einen enzymgekoppelten Immunadsorptionstest (ELISA) zum Nachweis des Bakteriums im Darm diagnostiziert.[5]. Eine Laboratoriumsdiagnose kann jedoch in der Regel nur eine nachträgliche Bestätigung der Infektion ermöglichen, da die Symptome der Erkrankung meist nach 24 Stunden bereits abgeklungen sind.[2]
Die Diagnose von Gasbrand wird zunächst klinisch gestellt.[1] Die Erregeranzucht kann aufgrund des zügigen Fortschreitens des Gasbrandes in der Regel nicht abgewartet werden und kann demzufolge lediglich der nachträglichen Bestätigung dienen.[6]
Mikrobiologischer Nachweis
Der Nachweis von Clostridium perfringens wird zunächst mikroskopisch durch Anfertigung eines gram-gefärbten Präparates geführt, in dem ca. 4 - 6 x 1 μm große Stäbchen mit abgerundeten Enden sichtbar werden. Dabei können in Originalpräparaten die Erreger teilweise von Kapseln umgeben sein, was an nicht angefärbten Zonen um die Bakterien erkennbar wird. Sporen sind gelegentlich in Stuhl- und Bodenproben zu finden, jedoch meist nicht in angezüchteten Kulturen. Als Merkmal dient u.a. die Unbeweglichkeit aufgrund der fehlenden Begeißelung und die fehlende Bildung von Sporen in vitro.
Des Weiteren wird das Verdachtsmaterial auf Anaerobier- bzw. Standard-Blutagar und auf Eigelb-Agar angezüchtet. Clostridium-perfringens-Kolonien werden unter Bebrütung in der Regel nach 10 bis 12 Stunden sichtbar. Charakteristisch sind beim Anaerobier-Blutagar runde, gewölbte, feuchtglänzende, gelegentlich rötlich schimmernde Kolonien von 3 bis 5 mm Durchmesser, die sich unter Sauerstoffeinwirkung erst grau, dann hellbraun und später grünlich verfärben und von keinem größeren Hämolysefeld umgeben sind. Auf dem Standard-Blutagar findet um die Kolonien eine Doppelzonenhämolyse statt. Auf Eigelb-Agar verursacht die vom Erreger freigesetzte Lecithinase eine charakteristische weißliche Aufhellung um den Wachstumsrasen („Seiffert-Nagler-Reaktion“). In Nährbouillons tritt rasch eine Trübung mit starker Gasentwicklung auf.
In Speziallaboratorien können zudem die Serotypen des Clostridium perfringens mittels Identifikation der Exotoxine in Tierversuchen unter Einsatz spezifischer Antiseren ermittelt werden.[3]
Einzelnachweise
- ↑ a b c d e f g h Rodloff, Arne C.: Obligat anaerobe sporenbildende Stäbchen, in: Hahn, Helmut et al. (Hrsg.): Medizinische Mikrobiologie und Infektiologie, 5. Aufl., Berlin/ Heidelberg 2004, S. 339ff.
- ↑ a b c Köhler, Werner: Sporenbildende gram-positive Bakterien (Bacillus, Clostridium) - Milzbrand, Tetanus, Gasbrand, pseudomembranöse Colitis, Botulismus, in: Ders. et al. (Hrsg.): Medizinische Mikrobiologie, 8. Aufl., Jena/ München 2001, S. 402ff.
- ↑ a b Ruckdeschel, Gerhard: Clostridium perfringens und andere histotoxische sowie sonstige, gewöhnlich apathogene Klostridienarten, in: Burkhardt, Friedrich (Hrsg.): Mikrobiologische Diagnostik, Stuttgart/ New York, S. 228ff.
- ↑ Finsterer, J./ Hess, B.: Neuromuscular and Central Nervous System Manifestations of Clostridium perfringens Infections, in: Infection (2007) 35, S. 396 - 405. [1]
- ↑ a b c Madigan, Michael T./ Martinko, John M.: Brock. Mikrobiologie, 11., überarb. Aufl., München et. al. 2006, S. 814.
- ↑ a b Hof, Herbert: Bakteriologie, in: Ders./ Dörries, Rüdiger (Hrsg.): Mikrobiologie (= Duale Reihe), Stuttgart 2005, S. 345ff.
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.