- Eschweiler-Clarke-Methylierung
-
Die Eschweiler-Clarke-Methylierung (oder einfach: Eschweiler-Clarke-Reaktion) ist eine chemische Reaktion aus dem Bereich der organischen Chemie. Sie wird zur Methylierung primärer oder sekundärer Amine verwendet und liefert tertiäre Amine. Sie ist benannt nach ihren Entwicklern Wilhelm Eschweiler und Hans Thacher Clarke.
Mechanismus
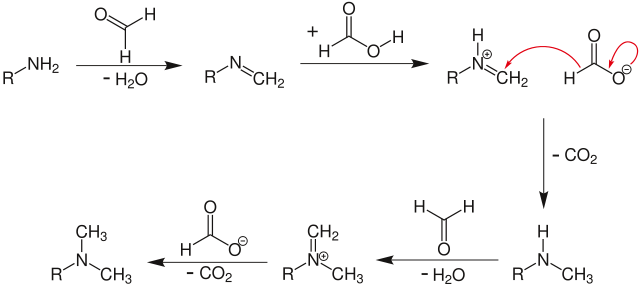
Als Methylierungsagens dient Formaldehyd, das im Überschuss zusammen mit überschüssiger Ameisensäure verwendet wird.[1][2] Im ersten Reaktionsschritt kondensiert Formaldehyd unter Abspaltung von Wasser an das eingesetzte Amin unter Bildung eines Imins. Dieses wird von der Ameisensäure zunächst am Stickstoff protoniert, dann findet der Übertrag eines Hydridions unter Bildung von Kohlenstoffdioxid statt. Der zweite Reaktionsschritt, der zur Bildung des zweifach methylierten Amins führt, folgt dem gleichen Mechanismus.
Die Triebkraft der Reaktion ist die Bildung von Kohlenstoffdioxid.Es erfolgt keine Bildung quartärer Ammoniumsalze, da aus den gebildeten tertiären Ammoniumverbindungen keine Imine mehr gebildet werden können. Hierin liegt ihr Vorteil gegenüber der Methylierung mit Halogenalkanen wie beispielsweise Methyliodid.
Werden chirale Amine eingesetzt, läuft die Reaktion meist unter Erhalt der Stereoinformation ab.[3]
Einzelnachweise
- ↑ W. Eschweiler in: Chem. Ber. 1905, 38, 880–882.
- ↑ H. T. Clarke, H. B. Gillespie, D. Z. J. Weisshaus in: J. Am. Chem. Soc. 1933, 55, 4571–4587.
- ↑ E. Farkas, C. J. Sunman in: Org. Chem. 1985, 50, 1110−1112.
Weblinks
Wikimedia Foundation.