- Fischer-Projektion
-
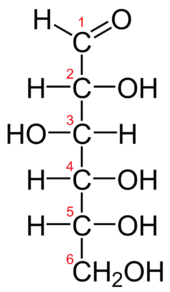 Beispiel: D-Glucose in der Fischer-Projektion
Beispiel: D-Glucose in der Fischer-Projektion
Die Fischer-Projektion ist eine Methode, die Raumstruktur einer chiralen chemischen Verbindung eindeutig zweidimensional abzubilden. Sie wurde von Emil Fischer entwickelt und verwendet die Stereodeskriptoren D (lat. dexter „rechts“) und L (lat. laevus „links“), die als Kapitälchen dargestellt und mit Bindestrichen von der übrigen Formel getrennt werden.
Inhaltsverzeichnis
Regeln
 Visualisierung der Fischer-Projektion: links oben die Keilstrichformel und rechts oben die Fischer-Projektion
Visualisierung der Fischer-Projektion: links oben die Keilstrichformel und rechts oben die Fischer-Projektion
Bei vielen chemischen Verbindungen ist die Stellung der Atome im Raum entscheidend für ihre Eigenschaften, was eine Unterscheidung verschiedener Stereoisomere notwendig macht. Vor allem bei Kohlenstoffverbindungen ist es oft schwierig, die räumliche Ausrichtung der bis zu vier Bindungspartner im Tetraederwinkel von 109,5° deutlich zu machen.
Die Fischer-Projektion löst dieses Problem ohne perspektivische Mittel durch Einhaltung folgender Regeln beim Zeichnen des Moleküls:
- Eine Kette von C-Atomen wird von oben nach unten gezeichnet, wobei das am stärksten oxidierte Atom oben steht. (Nach den Regeln über die Nomenklatur der Kohlenwasserstoffe steht das Kohlenstoffatom mit der Nummer 1 oben. Dies muss nicht immer das am stärksten oxidierte Kohlenstoffatom sein, ist es aber in den meisten Fällen[1]). Es gibt aber auch vereinbarte Ausnahmen wie z. B. die Galacturonsäure, die formal eine oxidierte Form der D-Galactose ist. Das höchst oxidierte Kohlenstoffatom ist in diesem Fall das C-Atom mit der Nr. 6, und man hält an der Nummerierung der D-Galactose fest.
- Horizontale (waagerechte) Linien zeigen aus der Projektionsebene hinaus auf den Betrachter zu. Dies kann auch durch ausgefüllte, zum Zentrum hin dünner werdende Keile angedeutet werden.[2]
- Vertikale (senkrechte) Linien laufen hinter die Projektionsebene, vom Betrachter weg. Dies kann auch durch quergestrichelte, zum Zentrum hin dünner werdende Keile angedeutet werden.[2]
Außerdem ist der Kohlenstoff das implizite Atom, d. h., das „C“ wird insbesondere in den Chiralitätszentren nicht geschrieben.
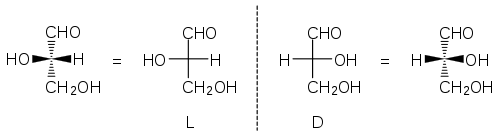
Als Beispiel sind die Fischerprojektionen der beiden Enantiomeren des Glycerinaldehyds angegeben, sowie die entsprechenden Keilstrichformeln. Mit den Stereodeskriptoren D und L wird dann die Konfiguration des untersten Stereozentrums angegeben, je nachdem, ob derjenige horizontale Rest mit der höheren Priorität (hier: OH > H) nach rechts (D) oder nach links (L) zeigt. Beim Vorliegen mehrerer Stereozentren kann man nicht mehrere Ds und Ls anhäufen (s. unten)
Es ist wichtig zu erwähnen, dass die tatsächliche räumliche Struktur chiraler Moleküle zur Zeit Fischers nicht bekannt war. Man verwendete den Glycerinaldehyd als Referenzsubstanz: Dem rechtsdrehenden Enantiomer wurde willkürlich die Projektion mit dem nach rechts zeigenden OH-Rest zugeteilt und diese daher als D-Konfiguration (lat. dexter: „rechts“) bezeichnet, ohne dass man wissen konnte, ob dies der Realität entsprach. Konnten andere Verbindungen (im Besonderen Zucker) zum rechtsdrehenden Glycerinaldehyd abgebaut werden, hatten sie unter dieser Annahme also auch D-Konfiguration.
1951 konnte Johannes Martin Bijvoet durch die Röntgenstrukturanalyse des Glycerinaldehyds die tatsächliche räumliche Struktur zeigen. Dabei stellte sich die willkürliche Annahme als richtig heraus: Die D- und R-Konfigurationen des Glycerinaldehyds sind identisch. Die D/L- und R/S-Konfiguration hat aber nichts mit dem optischen Drehsinn zu tun; so ist beispielsweise bei der Weinsäure das D-Enantiomer links- und das L-Enantiomer rechtsdrehend.
Liegen mehrere Stereozentren vor, können die Konfigurationen dieser nicht (wie beispielsweise bei der Cahn-Ingold-Prelog-Konvention) eine nach der anderen angegeben werden. Liegt mehr als ein Stereozentrum vor, gibt es mehr als zwei Stereoisomere, darunter Diastereomere und Enantiomere. Bei der Verwendung der Fischer-Nomenklatur ist es unumgänglich, Diastereomeren unterschiedliche Namen zu geben:
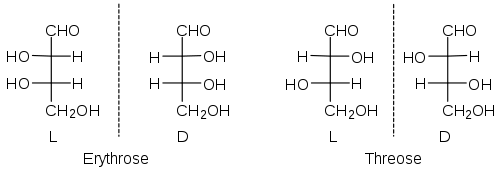
Erythrose und Threose sind beispielsweise zwei verschiedene Zucker, die sich nur durch die Konfigurationen an den beiden chiralen Zentren unterscheiden. Genauer, sie sind Diastereomere. Von beiden gibt es je ein Enantiomerenpaar. Die relative Konfiguration des oberen Stereozentrums wird also durch den Namen festgelegt: Bei der Erythrose zeigen die OH-Gruppen in die gleiche, bei der Threose in verschiedene Richtungen. Da aber z. B. C6-Aldosen (darunter die Glucose) 4 Stereozentren haben, gibt es 24 = 16 Stereoisomere. Das entspricht acht Enantiomerenpaaren, man muss sich also acht verschiedene Namen und acht verschiedene relative Konfigurationen für diese Gruppe von Zuckermolekülen merken.
Beispiel aus der Biochemie für D- und L-Verbindungen sind D-Glucose (Traubenzucker) und die Aminosäure L-Alanin.
Anwendung
Für ein Chiralitätszentrum
Es gibt auch eine Reihe von Regeln für die Interpretation einer Fischer-Projektion. Dadurch können Strukturen auf Isomerie untersucht werden, ohne sie sich dreidimensional vorstellen zu müssen, was oft sehr schwierig ist. Für eine Projektion mit einem zentralen Kohlenstoff und vier Substituenten gilt:
- Drehung um 180° (360°, …) ergibt dasselbe Molekül,
- Drehung um 90° (270°, …) ergibt das zugehörige Enantiomer.
- Eine (drei, fünf, …) Vertauschung(en) von je zwei Substituenten ergibt das Enantiomer,
- zwei (vier, sechs, …) Vertauschungen von je zwei Substituenten ergeben dasselbe Molekül.
Es sei erstens noch angemerkt, dass Kohlenstoffe, die nicht vier verschiedene Substituenten besitzen, sondern mindestens zwei gleiche oder eine Doppelbindung, nicht chiral sind und deshalb für die obigen Regeln überflüssig sind. Zweitens sei darauf hingewiesen – so trivial es auch erscheint –, dass der gesamte Substituent bei der Feststellung von Unterschiedlichkeit verglichen werden muss, d. h. wenn an der einen Seite eine Propylkette und an der anderen eine Ethylkette hängt, sind die Substituenten unterschiedlich.
Für mehrere Chiralitätszentren
Bei mehreren Chiralitätszentren gelten die Regeln genauso, und zwar für jedes einzelne Zentrum. Um die Isomerie eines Moleküls zu bestimmen, bietet sich die „Vertauschungsmethode“ an. Unterscheiden sich zwei Strukturen nur durch die Anordnung an den Chiralitätszentren, so gilt:
- Sie sind genau dann identisch, wenn jedes Zentrum identisch ist, also an jedem Zentrum zwei (oder auch null) Vertauschungen nötig sind, um die eine Struktur in die andere zu überführen,
- Sie sind genau dann Enantiomere, wenn das für jedes Zentrum gilt, also an jedem Zentrum eine Vertauschung nötig ist, um die eine Struktur in die andere zu überführen,
- Sie sind Diastereomere genau dann, wenn die beiden anderen Fälle nicht eintreten, d. h. zum Beispiel, wenn am einen Zentrum eine und am anderen zwei Vertauschungen nötig sind.
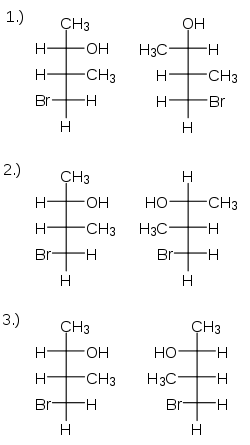
Als Beispiel soll das 1-Brom-2-methyl-butan-3-ol dienen:
Die Nummerierung gehe von unten nach oben. Das unterste Kohlenstoffatom, nummeriert als eins, ist achiral und dient nur der Verwirrung. Die Kohlenstoffe zwei und drei sind chiral. Im ersten Fall ist Zentrum zwei offenbar identisch, bei Zentrum drei sind zwei Vertauschungen nötig, es ist auch identisch: Die Moleküle sind identisch. Im zweiten Fall braucht man an Zentrum zwei eine, an Nummer drei zwei Vertauschungen: Es sind Diastereomere. Im dritten Fall liegt eine Spiegelung vor (an beiden Zentren eine Vertauschung), es sind Enantiomere.
meso-Formen
In der Fischer-Projektion kann man leicht eine Symmetrieebene und zwei Isomere als meso-Formen erkennen. Für eine Erläuterung sei auf den Artikel zu meso-Formen verwiesen.
Einzelnachweise
- ↑ Rules of Carbohydrate Nomenclature. In: The Journal of Organic Chemistry. 28, Nr. 2, 1963, S. 281–291, doi:10.1021/jo01037a001.
- ↑ a b Graphical representation of stereochemical configuration (IUPAC Recommendations 2006)
Siehe auch
- Sägebock-Projektion
- Newman-Projektion
- Keil-Strich-Schreibweise
- Haworth-Projektion
Weblinks
 Commons: Fischer projection – Sammlung von Bildern, Videos und Audiodateien
Commons: Fischer projection – Sammlung von Bildern, Videos und Audiodateien
Wikimedia Foundation.