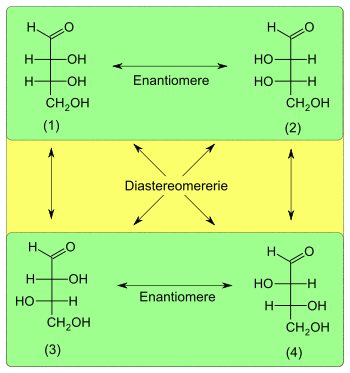
- Diastereomer
-
Diastereomere sind Stereoisomere (chemische Verbindungen gleicher Konstitution aber unterschiedlicher Konfiguration), welche sich – im Gegensatz zu Enantiomeren – nicht wie Bild und Spiegelbild verhalten. Diastereomere können sowohl chiral als auch achiral sein. Sie können sich in physikalischen (Schmelzpunkt, Siedepunkt, Löslichkeit usw.) und chemischen Eigenschaften voneinander unterscheiden und werden daher oftmals zur Trennung von chiralen Verbindungen mit chiralen Derivatisierungsreagenzien erzeugt.
Inhaltsverzeichnis
Diastereomerie aufgrund von Chiralität
Bei zwei Molekülen mit mehreren Stereozentren liegt Diastereomerie vor, wenn sie sich in einem, aber nicht allen Stereozentren unterscheiden. Ein Spezialfall der Diastereomerie ist die Epimerie. Hier unterscheiden sich die beiden Moleküle lediglich in einem Stereozentrum. Wenn hingegen die Konfiguration in allen Stereozentren zweier Verbindungen unterschiedlich ist, aber keine meso-Form vorliegt, liegen Enantiomere vor; Sie verhalten sich wie Bild und Spiegelbild. Enthält ein Molekül beispielsweise zwei Stereozentren und ist ein Stereozentrum gleich konfiguriert, das zweite jedoch unterschiedlich, so liegen Diastereomere vor, genauer gesagt Epimere. Diastereomere haben in der Regel unterschiedliche physikalische Eigenschaften (Schmelzpunkt, Siedepunkt, Löslichkeit, NMR-Spektrum, IR-Spektrum), während sich Enantiomere ausschließlich in ihrem Drehwert und in ihren chemischen Eigenschaften gegenüber anderen chiralen Molekülen und damit auch in ihren physiologischen Eigenschaften (Geruch, Geschmack) unterscheiden.
Ursache der Chiralität in einem Molekül sind meist Atome, die als Stereozentren bezeichnet werden. Meist handelt es sich um asymmetrisch substituierte Kohlenstoff-Atome, die vier unterschiedliche Reste tragen. An einem solchen Stereozentrum sind, bedingt durch die tetraedrische Struktur des C-Atoms, jeweils zwei Konfigurationen möglich, die auch durch Drehung nicht zur Deckung gebracht werden können. Um Diastereomere bilden zu können, müssen mehrere Chiralitätszentren vorhanden sein. Mit n Stereozentren ergeben sich dabei 2n verschiedene Verbindungen. Diastereomere mit mehreren Stereozentren sind meistens chiral. In bestimmten Fällen ergibt sich allerdings bei mehreren Stereozentren eine Spiegelebene im Molekül, wodurch diese sogenannte meso-Verbindung achiral wird.
Beispiel: D-Glucose und D-Galactose sind zwei Zucker, die sich in einem von vier Chiralitätszentren voneinander unterscheiden. Es handelt sich somit um Diastereomere und gleichzeitig um Epimere.
D-Glucose und L-Glucose unterscheiden sich in allen vier Stereozentren und verhalten sich wie Bild und Spiegelbild. Es sind also Enantiomere.
D-Glucose und L-Galactose unterscheiden sich in drei von vier Stereozentren. Es sind also Diastereomere, aber keine Epimere.π-Diastereomere
π-Diastereomere sind Isomere, die durch die Starrheit einer Doppelbindung aufgrund der π-Bindung bestehen. Doppelbindungen sowie die gebundenen Gruppen sind nicht frei drehbar. So existieren unterschiedliche räumliche Anordnungen. Beispiele sind die (E)- und (Z)-Isomere (veraltet cis- und trans-Isomere) der Alkene.
Diastereoselektivität
Chirale Moleküle differenzieren gegenüber anderen chiralen Molekülen zwischen den möglichen Enantiomeren. Das liegt daran, dass zwei verschiedene chirale Moleküle in einem diastereomeren Verhältnis zueinander stehen. Diastereoselektivität tritt in einer chemischen Reaktion sowohl zwischen zwei chiralen Edukten als auch zwischen einem chiralen Edukt oder Reagenz und einem prochiralen oder achiralen Edukt auf, so dass auf der Produktseite ein Enantiomer bevorzugt wird. Bei diastereoselektiven Reaktionen haben die verschiedenen Übergangszustände von Enantiomeren auch unterschiedliche physikalische Eigenschaften, woraus sich letztlich die Selektivität ergibt. Enantioselektive Synthesen beruhen letztlich immer auf diastereoselektiven Mechanismen, weshalb der Begriff Diastereoselektive Synthese zu bevorzugen ist. Eine einmal vorhandene Chiralität setzt sich somit in Folgesystemen fort.
Quellen
- Hans Beyer, Wolfgang Walter: Lehrbuch der Organischen Chemie. 19. völlig neu bearbeitete Auflage. S. Hirzel Verlag, Stuttgart 1981, ISBN 3-7776-0356-2.
- Hans Rudolf Christen, Fritz Vögtle: Organische Chemie. Von den Grundlagen zur Forschung. 2. Band. 2. Auflage. Otto Salle Verlag u. a., Frankfurt am Main 1996, ISBN 3-7935-5398-1.
- Karl Schwister (Hrsg.): Taschenbuch der Chemie. 4. aktualisierte Auflage. Fachbuchverlag Leipzig im Carl-Hanser-Verlag, München 2010, ISBN 978-3-446-42211-7
Wikimedia Foundation.