- Aminopyridine
-
Aminopyridine Name 2-Aminopyridin 3-Aminopyridin 4-Aminopyridin Andere Namen α-Aminopyridin
o-Aminopyridin
2-Pyridylamin
β-Aminopyridin
m-Aminopyridin
3-Pyridylamin
γ-Aminopyridin
p-Aminopyridin
4-Pyridylamin
Fampridin (INN)
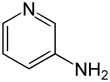
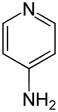
Dalfampridine (USAN)Strukturformel 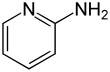
CAS-Nummer 504-29-0 462-08-8 504-24-5 PubChem 10439 10009 1727 Summenformel C6H6N2 Molare Masse 94,12 g·mol−1 Aggregatzustand fest Kurzbeschreibung farblose bis gelbliche, brennbare Kristalle mit unangenehmen Geruch Schmelzpunkt 55–58 °C[1] 60–63 °C[2] 158 °C[3] Siedepunkt 209–211 °C[1] 250–252 °C[2] 274 °C[3] pKs-Wert[4]
(der konjugierten
Säure BH+)6,71 6,03 9,114 Dichte 1,26 g·cm−3[3] Löslichkeit löslich in Wasser und Alkohol GHS-
Einstufung
Gefahr[5]
Gefahr[6]

Gefahr[7]
H- und P-Sätze 301-311-315-319-335 301-311-315
319-331-335-373300-315-319-335 keine EUH-Sätze keine EUH-Sätze keine EUH-Sätze 261-280-301+310
305+351+338-312261-280-301+310
305+351+338-311261-264-301+310
305+351+338Gefahrstoff-
kennzeichnung
[1][2][3]

Giftig Umwelt-
gefährlich(T) (N) 
Giftig (T) 
Sehr giftig (T+) R-Sätze 23/24/25-51/53 25-36/37/38 28-36/37/38 S-Sätze 26-36/37-45-61 26-28-37/39-45 (1)-28-37/39-45 Die Aminopyridine bilden in der Chemie eine Stoffgruppe von organischen Verbindungen, die zu den Heterocyclen (genauer: Heteroaromaten) zählt. Sie bestehen aus einem Pyridinring, der mit einer Aminogruppe (−NH2) substituiert ist. Aufgrund der unterschiedlichen Anordnung ergeben sich drei Konstitutionsisomere mit der Summenformel C6H6N2.
Inhaltsverzeichnis
Eigenschaften
Die Aminopyridine sind farblose bis gelbliche Feststoffe mit einem pyridinartigen Geruch. Sie sind löslich in Wasser und Alkoholen. Das 4-Aminopyridin, das die höchste Symmetrie aufweist, besitzt den höchsten Schmelzpunkt.
Verwendung
4-Aminopyridin wird zur Herstellung von 4-Halogenpyridinen und Arzneimitteln verwendet. Es selbst dient als Vogelgift[8] und in der Medizin als reversibler Kaliumkanalblocker (z.B. bei Multipler Sklerose).[9]
4-Aminopyridin wurde 2010 von der US-amerikanischen Arzneimittelbehörde unter dem US-amerikanischen Freinamen (USAN) Dalfampridine zur unterstützenden Behandlung der Multiplen Sklerose zugelassen.[10] Ein entsprechender Antrag für die Europäische Union wurde jedoch aufgrund eines ungenügenden Nutzen-Risiko-Verhältnisses vorläufig abgewiesen.[11] Eine Entscheidung der Schweizer Behörde steht noch aus.
Verwandte Verbindungen
- Diaminopyridine C5H7N3
- Triaminopyridine C5H8N4
- Methylaminopyridine C6H8N2
- Dimethylaminopyridine C7H10N2
Einzelnachweise
- ↑ a b c Eintrag zu 2-Aminopyridin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 16. März 2009 (JavaScript erforderlich).
- ↑ a b c Eintrag zu 3-Aminopyridin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 16. März 2009 (JavaScript erforderlich).
- ↑ a b c d Eintrag zu 4-Aminopyridin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 16. März 2009 (JavaScript erforderlich).
- ↑ CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- ↑ Datenblatt 2-Aminopyridine bei Sigma-Aldrich, abgerufen am 26. April 2011.
- ↑ Datenblatt 3-Aminopyridine bei Sigma-Aldrich, abgerufen am 26. April 2011.
- ↑ Datenblatt 4-Aminopyridine bei Sigma-Aldrich, abgerufen am 26. April 2011.
- ↑ US Environmental Protection Agency (27. September 2007): Reregistration Eligibility Decision for 4-aminopyridine. EPA 738-R-07-013. Zugegriffen am 2. Februar 2011.
- ↑ Goodman AD, Brown TR, Krupp LB, Schapiro RT, Schwid SR, Cohen R, Marinucci LN, Blight AR: „Sustained-release oral fampridine in multiple sclerosis: a randomised, double-blind, controlled trial“, in: Lancet, 2009, 373, S. 732–738; PMID 19249634.
- ↑ U.S. Food and Drug Administration. FDA Approves Ampyra to Improve Walking in Adults with Multiple Sclerosis (FDA News Release vom 22. Januar 2010). Abgerufen am 26. Januar 2010.
- ↑ Europäische Arzneimittelagentur (20. Januar 2011): Refusal of the marketing authorisation for Fampyra (fampridine). Zugegriffen am 30. Januar 2011.
Kategorien:- Giftiger Stoff
- Umweltgefährlicher Stoff
- Stoffgruppe
- Aminopyridin
Wikimedia Foundation.
