- K2S
-
Kristallstruktur 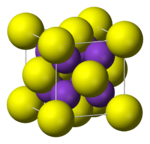
Allgemeines Name Kaliumsulfid Andere Namen - Dikaliummonosulfid
- Dikaliumsulfid
- Kaliummonosulfid
- Kalium Sulfuratum
Verhältnisformel K2S CAS-Nummer 1312-73-8 ATC-Code A12BA
Kurzbeschreibung hygroskopische, weiße Substanz oder farblose Kristalle Eigenschaften Molare Masse 110,26 g/mol Aggregatzustand fest
Dichte 1,805 g/cm3 (14 °C)[1]
Schmelzpunkt 840 °C[1]
Siedepunkt Zersetzung[1]
Löslichkeit leicht löslich in Wasser[1]
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 

Ätzend Umwelt-
gefährlich(C) (N) R- und S-Sätze R: 31-34-50 S: (1/2)-26-45-61 Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln WGK 2 (wassergefährdend)[1] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Kaliumsulfid ist ein Kaliumsalz des Schwefelwasserstoffs (H2S).
Inhaltsverzeichnis
Eigenschaften
Kaliumsulfid ist leichtentzündlich. Bei Luftkontakt kann es zur spontanen Selbstentzündung kommen. Erschütterung oder Reibung können zur Explosion führen. Der Kontakt mit Säuren führt zur Freisetzung von giftigem Schwefelwasserstoff. Mit Oxidationsmitteln entsteht Schwefeldioxid. An der Luft wandelt sich Kaliumsulfid allmählich in Kaliumthiosulfat um.
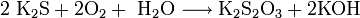
Wässrige Lösungen von Kaliumsulfid sind stark basisch und reagieren heftig mit Säuren.
Darstellung
Eine mögliche Darstellungsmethode ist die Sättigung einer Kaliumhydroxidlösung mit Schwefelwasserstoff. In der Lösung bildet sich Kaliumhydrogensulfid, dass sich mit einer äquivalenten Menge Kalilauge zu Kaliumsulfid umsetzen lässt.
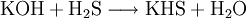
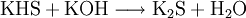
Aus der Lösung kristallisiert das Salz mit 5 mol Kristallwasser. Die grobe Entwässerung geht mit einer teilweisen Zersetzung einher. Die bei Natriumsulfid angegebene Methode ist erfolgreich.[3]
Prinzipiell lässt sich Kaliumsulfid auch durch das Zusammenschmelzen von Schwefel und Kaliumcarbonat gewinnen. Das braune Mischprodukt (Schwefelleber) wird im Handel zwar auch als Kaliumsulfid angeboten, enthält neben diesem aber zusätzlich Kaliumpolysulfide, Kaliumthiosulfat und Kaliumsulfat.
Toxikologie
Auf Haut, Augen und Atemwege wirkt Kaliumsulfid ätzend. Je nach Exposition kommt es äußerlich zu Rötungen, Blasenbildung und Verbrennungserscheinungen. Verschlucken hat Übelkeit, Erbrechen, Durchfall und Koliken zur Folge. Übelkeit und Erbrechen treten auch bei Inhalation auf. Hinzu kommt ein starker Hustenreiz, Halsschmerzen, Kopfschmerzen. Im schlimmsten Fall kann sich ein Lungenödem bilden.
Quellen
- ↑ a b c d e Eintrag zu Kaliumsulfid in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 3.9.2007 (JavaScript erforderlich)
- ↑ Eintrag zu CAS-Nr. 1312-73-8 im European chemical Substances Information System ESIS
- ↑ G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry 2nd ed., vol. 1, Academic Press 1963, S. 360-1.
Wikimedia Foundation.
