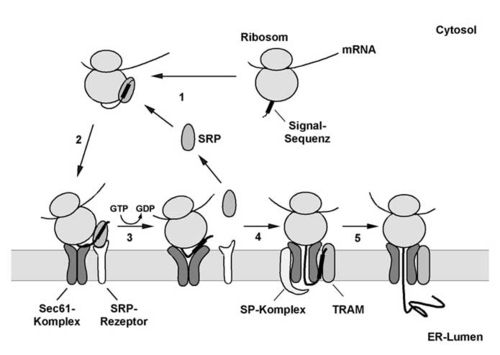
- Kotranslationaler Mechanismus
-
Der Cotranslationale Proteintransport (auch cotranslationale Translokation genannt) ist ein Begriff aus der Biochemie und der Zellbiologie und bezeichnet den Vorgang, bei dem Proteine während ihrer Synthese durch oder in eine Membran transportiert werden. Er grenzt sich ab zum posttranslationalen Proteintransport, bei dem die Proteinsequenz erst vollständig gebildet wird und anschließend durch oder in eine Membran transportiert wird.
Vorkommen
Bei Eukaryoten kommt cotranslationaler Proteintransport vor allem bei Transport durch oder in die Membran des Endoplasmatischen Retikulums (ER) vor. Durch Vesikeltransport können sich die membrangebundenen Proteine in die Membranen anderer Organellen oder in die Cytoplasmamembran verteilen. Die aus diesem Grund an der ER-Membran sitzenden Ribosomen geben dem rauen ER seinen Namen.
Bei Prokaryoten kommt cotranslationaler Proteintransport an der Cytoplasmamembran vor.
Mechanismus
Der Transportprozess beginnt mit der spezifischen Erkennung der N-terminalen Signalsequenz. Sobald die Signalsequenz an der Oberfläche des Ribosoms erscheint, wird sie vom Signalsequenzerkennungspartikel (SRP) gebunden, das im Säuger aus sechs Proteinen und einer 7SL-RNA besteht. Das gebundene SRP interagiert dabei nicht nur mit der Signalsequenz, sondern auch mit dem Ribosom, wodurch die Synthesegeschwindigkeit der naszierenden Polypeptidkette drastisch herabgesetzt wird. Das SRP ist somit in der Lage, das Ribosom zur ER-Membran zielzuleiten, ohne dass vorher das zu transportierende Protein fertiggestellt wird. An der ER-Membran angelangt, interagiert der Komplex aus Ribosom, naszierender Peptidkette und SRP auf zweifache Weise mit der Membran. Zum einen wird das SRP von seinem membranständigen Rezeptor (SRP-Rezeptor) gebunden, zum anderen interagiert das Ribosom direkt mit dem tunnelbildenden Sec61-Komplex. Nachdem SRP und SRP-Rezeptor aneinander gebunden haben, löst sich das SRP unter GTP-Hydrolyse vom Ribosom und übergibt die naszierende Polypeptidkette an den eigentlichen Translokationsapparat.
Im Säugersystem konnte in Rekonstitutionsexperimenten gezeigt werden, dass neben dem SRP-Rezeptor nur noch zwei weitere Komponenten in der Membran benötigt werden, um Proteine in vitro cotranslational zu transportieren. Es handelt sich dabei um das TRAM-Protein (translocating chain-associated membrane protein) und um den heterotrimeren Sec61-Komplex. Quervernetzungsexperimente sowie elektronenmikroskopische Untersuchungen zeigten, dass der Sec61-Komplex den Kanal bildet, durch den die Proteine hindurchtransportiert werden. Der Kanal wird dabei von 3 bis 4 heterotrimeren Sec61-Komplexen gebildet, die im elektronenmikroskopischen Bild als ringförmige Struktur erscheinen. Die Insertion der naszierenden Kette in den Translokationskanal erfolgt in zwei Schritten. Zu Beginn des Translokationsprozesses ist die Bindung zwischen Sec61-Komplex und Ribosom relativ schwach. Die Ribosomen können durch eine Hochsalzbehandlung von der Membran abgewaschen werden. Erst wenn die naszierenden Kette eine Länge von ca. 70 Aminosäuren erreicht hat und eine funktionelle Signalsequenz vorhanden ist, wird die Bindung zwischen Ribosom und Sec61-Komplex hochsalzresistent. Gleichzeitig öffnet sich der Translokationskanal zur luminalen Seite des ER. Durch elektronenmikroskopische Aufnahmen konnte gezeigt werden, dass das Ribosom so auf der Membranpore sitzt, dass der Sec61-Kanal eine Verlängerung des Ribosomenkanals darstellt. Die GTP-abhängige Synthese der naszierenden Kette am Ribosom reicht als alleinige Kraft aus, um die naszierende Polypeptidkette ins Lumen des ER zu transportieren.
- Die Signalsequenz der wachsenden Polypeptidkette wird vom SRP erkannt und gebunden. Gleichzeitig interagiert das SRP auch mit dem Ribosom, wodurch es zu einem Elongationsarrest kommt.
- Der Komplex aus Ribosom, naszierender Polypeptidkette und SRP bindet an die ER-Membran, wobei das SRP mit seinem membranständigen Rezeptor und das Ribosom mit dem Sec61-Komplex interagiert.
- Unter GTP-Hydrolyse wird die Signalsequenz vom SRP auf den Sec61-Komplex übertragen. Es erfolgt ein zweiter Signalsequenz-erkennungsschritt durch den Sec61-Komplex.
- Der Translokationskanal öffnet sich zum ER-Lumen. Der N-Terminus der naszierenden Kette liegt in einer Haarnadelkonformation vor, wobei der eine Teil der Schleife von der Signalsequenz und der andere Teil von den C-terminal nachfolgenden Abschnitten der Polypeptidkette gebildet wird. Die Signalsequenz interagiert dabei mit Sec61a, TRAMp und Membranlipiden. Durch die weitere Elongation der Polypeptidkette wird der C-terminale Bereich der Schleife durch die Membran geschoben. Die Signalsequenz wird dabei vom restlichen Protein durch den Signalpeptidase-Komplex (SP-Komplex) abgespalten.
- Anschließend wird die restliche naszierende Polypeptidkette direkt durch den von Ribosom und Sec61-Komplex gebildeten Kanal ins Lumen des ER transportiert.
Wikimedia Foundation.