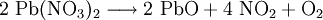- Pb(NO3)2
-
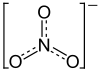
Strukturformel 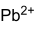
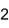
Allgemeines Name Blei(II)-nitrat Andere Namen Bleinitrat
Summenformel Pb(NO3)2 CAS-Nummer 10099-74-8 Kurzbeschreibung weißer, pulvriger Feststoff Eigenschaften Molare Masse 331,21 g/mol Aggregatzustand fest
Dichte 4,53 g/cm3[1]
Schmelzpunkt Siedepunkt Zersetzt sich vor dem Sieden[1]
Löslichkeit gut (522 g/l) in Wasser[1]
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 

Giftig Umwelt-
gefährlich(T) (N) R- und S-Sätze R: 61-20/22-33-62-50/53 S: 53-45-60-61 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Blei(II)-nitrat, ein weißer, pulvriger Feststoff, ist das Blei(II)-salz der Salpetersäure. Seine molare Masse beträgt 331,23 g/mol, die Dichte seiner Kristalle 4,53 g/cm3. Blei(II)-nitrat ist ein starkes Oxidationsmittel. Es ist im Gegensatz zu anderen Bleisalzen gut in Wasser löslich. Aus diesem Grund ist es sehr giftig.
Inhaltsverzeichnis
Darstellung
Blei(II)-nitrat entsteht bei der Reaktion von heißer, verdünnter Salpetersäure mit (1) Blei oder (2) Blei(II)-oxid:
Aus den Lösungen kristallisiert es in großen, wasserklaren Kristallen aus.
Die Umsetzung von Blei(II)-carbonat mit Salpetersäure liefert ebenso Blei(II)-nitrat unter Bildung von Kohlenstoffdioxid:
Eigenschaften
Im Gegensatz zu vielen anderen Blei(II)-salzen wie Blei(II)-chlorid oder Blei(II)-sulfat ist Blei(II)-nitrat gut in Wasser löslich.
Erhitzt man Blei(II)-nitrat bis zu seiner Zersetzungstemperatur von 470 °C, so wandelt es sich unter Bildung von Stickstoffdioxid und Sauerstoff in Blei(II)-oxid um:
Daher ist diese chemische Reaktion im Labor zur Bildung geringer Mengen des Gases Stickstoffdioxid geeignet. Wegen der Sauerstoff-Freisetzung wird Blei(II)-nitrat bei der Synthese von Farbstoffen als Oxidationsmittel eingesetzt.
Toxizität
Bleinitrat kann über die Haut aufgenommen werden, beeinträchtigt die Fortpflanzungsfähigkeit und ist möglicherweise carcinogen (als krebserregend Kat. III eingestuft). Schülerexperimente mit Bleinitrat sind problematisch.
Verwendung
Verwendung findet Blei(II)-nitrat weiterhin bei der Herstellung von Textilbeizen, Streichhölzern, Spezialexplosivstoffen, Ätzlösungen und zur Perlmuttfärbung.
Quellen
Wikimedia Foundation.

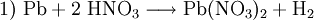
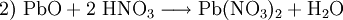
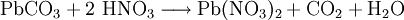
_nitrate_1.jpg)