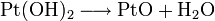- Platinmonoxid
-
Kristallstruktur Keine Kristallstruktur vorhanden Allgemeines Name Platin(II)-oxid Andere Namen Platinmonoxid
Verhältnisformel PtO CAS-Nummer 12035-82-4 Kurzbeschreibung schwarzes Pulver Eigenschaften Molare Masse 211,08 g·mol−1 Aggregatzustand fest
Dichte 14,9 g·cm−3[1]
Schmelzpunkt Löslichkeit Unlöslich in Wasser oder Ethanol, löslich in Königswasser[1]
Sicherheitshinweise Gefahrstoffkennzeichnung 
unbekannt R- und S-Sätze R: ? S: ? Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Platin(II)-oxid (auch Platinmonoxid) ist eines von mehreren Oxiden des chemischen Elementes Platin. Daneben existieren noch Platin(IV)-oxid und Platin(VI)-oxid.
Inhaltsverzeichnis
Gewinnung und Darstellung
Platin(II)-oxid lässt sich durch Erhitzen von Platin auf 430 °C in einer Sauerstoff-Atmosphäre mit erhöhten O2-Druck gewinnen. Platin(IV)-oxid zerfällt ab 400 °C zu Platin(II)-oxid und Sauerstoff.
Es kann auch durch vorsichtiges Erhitzen von Platin(II)-hydroxid unter Abspaltung von Wasser gewonnen werden:[1]
Eigenschaften
Platin(II)-oxid kristallisiert wie Palladium(II)-oxid nicht in einer Natriumchlorid-, sondern in einer Platinsulfid-Struktur. In dieser liegen kantenverknüpfte Quadrate einer PtO4-Struktur vor. Daneben sind die Platin- und Sauerstoffatome in Bändern angeordnet.
Mit Ausnahme von Königswasser ist Platin(II)-oxid in Säuren unlöslich. Als starkes Oxidationsmittel wird es auch von schwachen Reduktionsmitteln wie Wasserstoff bei Raumtemperatur zum Element reduziert.
Das durch Reaktion von Platin(II)-lösungen mit Natronlauge gebildete Platinmonoxid-hydrat lässt sich nicht ohne Sauerstoffabgabe zu Platin(II)-oxid dehydratisieren. Versucht man es unter Anwesenheit von Sauerstoff zu entwässern, bildet sich stattdessen ein Platin(III)-oxid-hydrat.
Einzelnachweise
- ↑ a b c d Simon Cotton: Chemistry of Precious Metals, 1997, Seite 725
- ↑ Arnold F. Holleman, Nils Wiberg: Lehrbuch der Anorganischen Chemie, 102. Auflage, de Gruyter, Berlin 2007, S. 1732, ISBN 978-3-11-017770-1.
Literatur
- Arnold F. Holleman, Nils Wiberg: Lehrbuch der Anorganischen Chemie, 102. Auflage, de Gruyter, Berlin 2007, S. 1732–34, ISBN 978-3-11-017770-1.
Wikimedia Foundation.