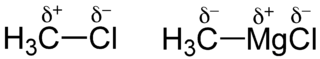- Polarität (Chemie)
-
Polarität bezeichnet in der Chemie eine durch Ladungsverschiebung in Atomgruppen entstandene Bildung von getrennten Ladungsschwerpunkten, die bewirken, dass eine Atomgruppe nicht mehr elektrisch neutral ist (siehe auch Pol). Das elektrische Dipolmoment ist ein Maß für die „Polarität“ des Moleküles.
Inhaltsverzeichnis
Polare Stoffe
Ein polarer Stoff besteht aus polaren Molekülen, welche sich durch ein permanentes elektrisches Dipolmoment auszeichnen.
Polare Stoffe lösen sich gut in polaren Lösungsmitteln (wie z. B. Salze in Wasser). Die Löslichkeit ist umso besser, je ähnlicher die Wechselwirkungskräfte zwischen den Teilchen des Lösungsmittels und zwischen denen des gelösten Stoffes sind.
Überschreitet der Unterschied in der Elektronegativität (ΔEN) einen gewissen Grenzwert (ca. 1,7), so gehen die Bindungselektronen komplett von einem Bindungspartner zum anderen über. Es verbleiben zwei Ionen, welche sich nur noch aufgrund der ungerichteten elektrostatischen Coulombkraft anziehen. Ionen sind als Ladungsträger grundsätzlich „polar“, d. h. Salze sind stets polare Stoffe.
Die Polarität eines gesamten Moleküls wird durch polare Atombindungen, oder im Extremfall durch ionische Bindungen hervorgerufen. Polare Bindungen zeichnen sich durch ungleichmäßige Verteilung von Bindungselektronen zwischen den Bindungspartnern aus. Verbinden sich Atome mit unterschiedlicher Elektronegativität, so resultiert eine solche Polarisierung der Bindung. Liegen in einem Molekül nur polarisierte Atombindungen vor, so addieren sich die einzelnen Dipolmomente der Bindungen vektoriell zu einem Gesamtdipolmoment. Ist dieses symmetriebedingt null, so ist der Stoff unpolar (Bsp. CO2). Liegt jedoch ein permanentes Gesamtdipolmoment ungleich null vor, so ist das Molekül polar (Beispiel: Wassermolekül). Je nach Größe dieses Gesamtdipolmoments ist ein Stoff mehr oder weniger polar. Der Unterschied geht von daher fließend von extrem polar bis komplett unpolar. Lösungsmittel werden anhand ihrer Polarität in einer elutropen Reihe geordnet.
In der organischen Chemie spielen polare Atombindungen eine wichtige Rolle bei der qualitativen Abschätzung der Reaktivität eines Moleküls. In einem Halogenalkan (Beispiel: Chlormethan) wird z. B. dem kovalent an das Kohlenstoffatom gebundene Chloratom die Partialladung δ− und dem Kohlenstoffatom der Methylgruppe die Partialladung δ+ zugewiesen. Setzt man Chlormethan mit Magnesium zur entsprechenden Grignard-Verbindung CH3MgCl um, tritt Umpolung ein: Das Kohlenstoffatom der Methylgruppe besitzt nun die Partialladung δ−. Aus der Polaritätsbetrachtung von organischen Stoffen ergeben sich wesentliche Konsequenzen für deren Reaktivität.
Beispiele:
Unpolare Stoffe
Ein unpolares oder apolares Molekül dagegen besitzt kein permanentes Dipolmoment.
Unpolare Stoffe lösen sich gut in unpolaren Lösungsmitteln (organische Stoffe in Benzol oder Ether). Die Löslichkeit ist umso besser, je ähnlicher die Wechselwirkungskräfte zwischen den Teilchen des Lösungsmittels und zwischen denen des gelösten Stoffes sind.
Beispiele:
Das Dipolmoment eines Stoffes bestimmt seine Löslichkeit oder seine Fähigkeit, als Lösungsmittel zu wirken. Dabei gilt die Faustregel, dass polare Stoffe in polaren Lösungsmitteln gut, in unpolaren aber schlecht löslich sind. Unpolare Stoffe wiederum sind in unpolaren Lösungsmitteln (z. B. Benzin, Hexan) gut, in polaren aber schlecht löslich. Dies wurde von den mittelalterlichen Alchemisten mit der Regel „similia similibus solvuntur“ (lat: „Ähnliches wird von Ähnlichem gelöst“) beschrieben.
Auch sind viele Salze im polaren Lösungsmittel Wasser auf Grund ihrer Ionenstruktur gut löslich, unpolare Stoffe wie Fett oder Wachs dagegen nicht.
Viele Aromastoffe oder Duftstoffe sind beispielsweise in Wasser nicht löslich und werden daher in einem Öl gelöst oder in Alkohol, deshalb ist Alkohol auch in vielen Lebensmitteln als Zutat aufgeführt.
Ein einfaches Experiment, mit dem man feststellen kann, dass Wasser ein permanentes elektrisches Dipolmoment besitzt, ist das Folgende:
Man lädt z.B. einen Kunststoffkamm durch das Kämmen trockener Haare oder Reiben an einem Wollpullover elektrisch auf. Nun lässt man aus einem Wasserhahn einen ganz dünnen Strahl fließen, gerade so dass er nicht abreißt und tropft. Wenn man nun den Kamm dem Wasserstrahl vorsichtig nähert, macht dieser einen Bogen und nähert sich dem Kamm. Dabei darf der Wasserstrahl aber den Kamm nicht berühren, da der Kamm ansonsten entladen wird.Die Erklärung für dieses Verhalten ist einfach: In dem inhomogenen elektrischen Feld richten sich die Dipole des Wassermoleküls so aus, dass sie zum Kamm hin zeigen. Auf das dem Kamm nähere Molekülende wirkt aufgrund des inhomogenen Feldes eine größere anziehende Kraft als die abstoßende Kraft auf das andere Molekülende. Insgesamt bleibt also eine kleine anziehende Kraft für jedes Wassermolekül übrig, die dann den Wasserstrahl umlenkt.
Bestimmung der Polarität
Um zu bestimmen, ob eine Verbindung unpolar, polar oder sogar eine Ionenbindung ist, kann man die Elektronegativitätsdifferenz ΔEN verwenden. Sie ist die Differenz der Elektronegativitätswerte der beteiligten Atome. Richtwerte für diese Einteilung sind in der unten dargestellten Tabelle zu sehen.
Dabei muss allerdings berücksichtigt werden, dass ladungsgetrennte mesomere Grenzformeln ein nicht zu vernachlässigendes Gewicht haben können. So ist Kohlenmonoxid trotz einer Elektronegativitätsdifferenz von etwa 1 ein nahezu unpolares Gas, das erst unterhalb von −140 °C durch Druck verflüssigt werden kann.
Richtwerte für die Einteilung der Polarität einer Bindung ΔEN Bindungsart Kennzeichen der Bindung 0,0 unpolare Bindung Elektronenpaare werden von allen Atomen gleich stark beansprucht, sodass keine Ladungsschwerpunkte entstehen. 0,1…0,4 schwach polare Bindung Ein Atom beansprucht Elektronenpaare stärker als das andere. 0,4…1,7 stark polare Bindung Ein Atom beansprucht Elektronenpaare noch stärker als das andere. > 1,7 Ionenbindung Es sind keine gemeinsamen Elektronenpaare vorhanden, d. h., es bilden sich Ionen Siehe auch
Wikimedia Foundation.