- Mellitsäure
-
Strukturformel 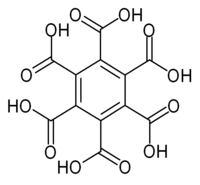
Allgemeines Name Mellitsäure Andere Namen - Benzolhexacarbonsäure
- Graphitsäure
- Mellithsäure
Summenformel C12H6O12 CAS-Nummer 517-60-2 PubChem 2334 Kurzbeschreibung feine seidige Nadeln
Eigenschaften Molare Masse 342,16 g·mol−1 Aggregatzustand fest
Schmelzpunkt pKs-Wert Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [1] 
Achtung
H- und P-Sätze H: 315-319-335 EUH: keine EUH-Sätze P: 261-305+351+338 [1] EU-Gefahrstoffkennzeichnung [1] 
Reizend (Xi) R- und S-Sätze R: 36/37/38 S: 26-36 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Mellitsäure (Benzolhexacarbonsäure, auch Graphitsäure) ist eine Säure, die erstmals im Jahr 1799 von Martin Heinrich Klaproth im Mineral Mellit (Honigstein) entdeckt wurde, dem Aluminiumsalz der Säure.
Inhaltsverzeichnis
Darstellung
Mellitsäure kann durch Erwärmen von Mellit mit Ammoniumcarbonat hergestellt werden. Mit einem Überschuss von Ammoniak werden die Aluminiumionen als Hydroxid ausgefällt und abgetrennt; es verbleibt das Ammoniumsalz der Mellitsäure. Die Säure kann auch durch Oxidation von reinem Kohlenstoff oder Hexamethylbenzol hergestellt werden, in der Kälte durch alkalisches Kaliumpermanganat oder durch heiße konzentrierte Salpetersäure.[3]
Eigenschaften
Mellitsäure kristallisiert in feinen seidigen Nadeln und ist in Wasser und Ethanol löslich. Es ist eine sehr stabile Verbindung: Chlor, konzentrierte Salpetersäure und Iodwasserstoff haben keine zersetzende Wirkung. Mellitsäure zersetzt sich durch trockene Destillation in Kohlenstoffdioxid und Pyromellitsäure, C10H6O8; in Gegenwart von Kalk erfolgt vollständige Zersetzung in Kohlenstoffdioxid und Benzol. Eine Umsetzung der Säure mit überschüssigem Phosphorpentachlorid bildet das Säurechlorid, das in Nadeln kristallisiert und bei 190 °C schmilzt.
Die hohe Stabilität der Mellitsäuresalze und ihre Eigenschaft als Endprodukt der Oxidation von polycyclischen aromatischen Kohlenwasserstoffen, die im Sonnensystem vorkommen, machen sie zu möglichen Kandidaten für organische Substanzen im Marsboden.[4]
Literatur
- Henry Enfield Roscoe, Carl Schorlemmer: "Mellitene Group", A Treatise on Chemistry: Vol. II: The Chemistry of the Hydrocarbons and their Derivatives on Organic Chemistry: P.V:529. D. Appleton and Co. (1889).
Einzelnachweise
- ↑ a b c d Datenblatt Mellitic acid bei Sigma-Aldrich, abgerufen am 9. April 2011.
- ↑ a b c d e f CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- ↑ Reaktionen des Kohlenstoffs bei webelements.com
- ↑ S. A. Benner, K. G. Devine, L. N. Matveeva, D. H. Powell: "The missing organic molecules on Mars", in: Proceedings of the National Academy of Sciences, 2000, 97 (6), S. 2425–2430; doi:10.1073/pnas.040539497; PMID 10706606.
Kategorien:- Reizender Stoff
- Benzolcarbonsäure
Wikimedia Foundation.
