- Sinistrin
-
Strukturformel 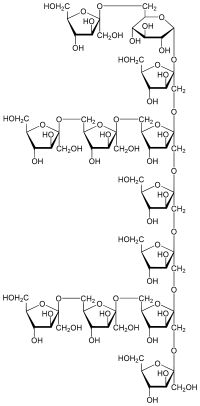
Eine mögliche Struktur von SinistrinAllgemeines Name Sinistrin Andere Namen - Polyfructosan
- Polyfructosan-S
- Inulin-Analog
- Inutest
CAS-Nummer 37311-25-4 ATC-Code V04CH01
Kurzbeschreibung schwach gelbgefärbtes, mehlartiges Pulver[1] Monomer Monomer Fructose Summenformel C6H10O6 Molare Masse 180,16 g·mol−1 Eigenschaften Aggregatzustand fest Schmelzpunkt Zersetzung bei 160–170 °C[1] Löslichkeit Sicherheitshinweise Gefahrstoffkennzeichnung [3] keine Einstufung verfügbar R- und S-Sätze R: siehe oben S: siehe oben Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Sinistrin (auch Polyfructosan) ist ein natürlich in vielen Pflanzen vorkommendes Polysaccharid. Sinistrin dient wie das ähnliche Fruktan Inulin als Energiespeicher (Speicherkohlenhydrat) der Pflanzen.
Inhaltsverzeichnis
Entdeckungsgeschichte und Herstellung
Schmiedeberg gelang 1879 die Isolation eines neuen Kohlenhydrats aus der Knolle der roten Meerzwiebel (Urginea maritima)[2][4]. Er gab der linksdrehenden Substanz den Namen „Sinistrin“, nach dem lateinischen Wort sinister für ‚links‘. Hammarsten fand das Sinistrin 1885 in Mucinen der Weinbergschnecke (Helix pomatia).[1] Heute wird Sinistrin in erster Linie aus der roten Meerzwiebel über mehrere Extraktions- und Reinigungsschritte industriell gewonnen.
Chemische Struktur und Eigenschaften
Sinistrin ist ein β–D-Fructan vom Inulin-Typ mit Verzweigungen an Position 6. Es zählt wie Inulin zu den Fruktanen bzw. wird teils auch zu den Fructooligosacchariden (FOS) gerechnet.[5][4] Sinistrin besteht zu ca. 97 % aus Fructose und ca. 3 % aus Glucose, wobei sich die Kette aus Fructosemolekülen zusammensetzt, die einen endständigen Glucoserest besitzen. Der Polymerisationsgrad von Sinistrin liegt durchschnittlich bei 15, das Molekulargewicht bei 3500 Da, mit einer Schwankungsbreite zwischen 2000 und 6000 Da[6][4].
Sinistrin unterscheidet sich von Inulin durch hohe Wasserlöslichkeit (auch in kaltem Wasser) und bessere Alkalistabilität. Beim Versetzen einer wässrigen Sinistrinlösung mit Kupfersulfat-Lösung und anschließend mit Kalilauge entsteht eine tiefblau gefärbte Lösung. Wird diese erhitzt, scheidet sich sofort ein hellblauer, flockiger Niederschlag ab; die Reaktion kann als empfindlicher Nachweis auf Sinistrin eingesetzt werden.[1] Mit Calciumhydroxid oder Kalkmilch bildet Sinistrinlösung einen Niederschlag[2].
Verwendung in der Medizin
Sinistrin wird wie Inulin in der physiologischen Forschung zur Bestimmung des extrazellulären Raums eingesetzt, da es leicht in das Interstitium eindringt, nicht jedoch in die Zellen. Sinistrin wird im Glomerulum vollständig filtriert, aber im Tubulus-System weder sezerniert noch reabsorbiert. Es wird daher unverändert und vollständig über die Nieren ausgeschieden. Die Messung der Sinistrin-Clearance wird daher zur exakten Bestimmung der glomerulären Filtrationsrate (GFR) der Nieren benutzt[7][8]. Diese Ausscheidungsrate gibt Auskunft über die Tätigkeit bzw. den Gesundheitszustand der Nieren. Die quantitative Bestimmung von Sinistrin in Harn und Plasma ist mit der von Inulin identisch. Für diesen Anwendungsbereich ist Sinistrin als wässrige Lösung unter dem Handelsnamen „Inutest“ als Arzneimittel zugelassen[9].
Literatur
- D.P. Mertz und H. Sarre: Polyfructosan-S: Eine neue inulinartige Substanz zur Bestimmung des Glomerulusfiltrates und des physiologisch aktiven extracellulären Flüssigkeitsvolumens beim Menschen. Klin Wochenschrift 1963;41:868-72.
Einzelnachweise
- ↑ a b c d e M. Geldmacher-Mallinckrodt und F. May: Die Polysaccharide der Weinbergschnecke II. Die Mucin-Polysaccharide der Eiweißdrüse. 1. Mitteil.: Die Identität von Galaktogen und Sinistrin. Hoppe-Seyler´s Zeitschrift für physiologische Chemie. Band 307, Heft 1-2, S. 191–201, ISSN (Online) 1437-4315, ISSN (Print) 0018-4888. doi:10.1515/bchm2.1957.307.1-2.191.
- ↑ a b c O. Schmiedeberg: Ueber ein neues Kohlehydrat. Hoppe-Seyler´s Zeitschrift für physiologische Chemie , Band 3 (1-2), 1879. doi:10.1515/bchm1.1879.3.1-2.112.
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ a b c Biopolymers, Polysaccharides II, Wiley-VCH, 2002, ISBN 3-527-30227-1.
- ↑ E. Nitsch, W. Iwanov und K. Lederer: Molecular characterization of Sinistrin. Carbohydrate Research 72 (1979) 1-12.
- ↑ T. Spies, W. Praznik, A. Hofinger, F. Altmann, E. Nitsch, R. Wutka: Carbohydr. Res. 235 (1992) 221–230.
- ↑ B. Watschinger und I. Kobinger: Wiener Zeitschrift für Innere Medizin 45 (1964) 219-228.
- ↑ T. Buclin, A. Pechere-Bertschi, R. Sechaud et al.: Sinistrin clearance for determination of glomerular filtration rate: a reappraisal of various approaches using a new analytical method. J Clin Pharmacol 1997;37:679–92. 204–211.
- ↑ Inutest 25% Ampullen (PDF) bei pharmazie.com, abgerufen am 7. Juli 2011.
Siehe auch
Wikimedia Foundation.
