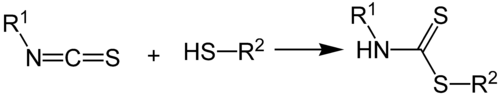- Dithiocarbamate
-
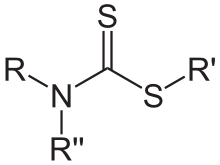
Als Dithiocarbamate (auch Dithiourethane genannt) werden Ester und Salze (bzw. deren Derivate) der Dithiocarbaminsäure bezeichnet und sind Di-Schwefel Analoga der Carbamate. Ihre allgemeine Struktur ist R–N(–R′′)–C(=S)–S–R′, wobei R, R′ und R′′ für austauschbare Reste stehen. Sie werden häufig in der Landwirtschaft als Fungizide, Herbizide und Insektizide, in der chemischen Industrie aber auch als Vulkanisationsbeschleuniger eingesetzt. Sie sind im allgemeinen schlecht löslich in Wasser aber gut löslich in organischen Lösungsmitteln. Sie entstehen bei der Reaktion von Kohlenstoffdisulfid mit Ammoniak und primären und sekundären Aminen.
Inhaltsverzeichnis
Synthese
Dithiocarbamate bilden sich aus Isothiocyanaten und Thioalkoholen durch eine Additionsreaktion:[1]
Derivate
- Dazomet C5H10N2S2, wird als Pflanzenschutzmittel eingesetzt
- Disulfiram C10H20N2S4, wird zur Behandlung von Alkoholismus eingesetzt
- Dithiocarb C5H10NS2Na, wird als Chelator eingesetzt, CAS: 148-18-5
- Ferbam C9H18FeN3S6, wird als Fungizid eingesetzt, CAS: 14484-64-1
- Mancozeb C4H6MnN2S4;C4H6ZnN2S4, wird als Fungizid eingesetzt,CAS: 8018-01-7
- Maneb C4H6N2S4·Mn, wird als Fungizid eingesetzt, CAS: 14484-64-1
- Metam C2H5NS2 bzw. Metamnatrium C2H5NS2Na , wird als Fungizid, Herbizid und Nematizid eingesetzt. CAS: 137-42-8
- Methyl-metiram C10H20N5S8Zn, wird als Pestizid eingesetzt, CAS: 8064-35-5
- Metiram C16H33N11S16Zn3 Mischfällung, wird als Fungizid eingesetzt, CAS: 9006-42-2
- Nabam C4H6N2Na2S4, wird als Herbizid, Algizid und Fungizid verwendet, ist als krebserregend eingestuft, CAS: 142-59-6[2]
- Propineb (C5H8N2S4Zn)x, wird als Fungizid eingesetzt, CAS: 12071-83-9
- Thiram (TMTD) C6H12N2S4, wird als Pestizid eingesetzt, CAS:137-26-8
- Zineb C4H6N2S4Zn, wird als Fungizid eingesetzt, CAS: 12122-67-7
- Ziram C6H12N2S4Zn, wird als Fungizid und Vulkanisationsbeschleuniger eingesetzt
Einzelnachweise
- ↑ Max Bögemann, Siegfried Petersen, Otto-Erich Schultz und Hanna Söll: Methoden zur Herstellung und Umwandlung von schwefelhaltigen Kohlensäurederivaten in Houben-Weyl: Methoden der Organischen Chemie, Band 9, Georg Thieme Verlag, Stuttgart, 1955, Seiten 773−915, dort Seite 831.
- ↑ Datenblatt der Carcinogenic Potency Database (englisch)
Weblinks
Wikimedia Foundation.