- Eisen(II,III)-oxid
-
Kristallstruktur 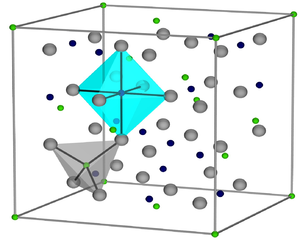
Allgemeines Name Eisen(II,III)-oxid Andere Namen - Trieisentetraoxid
- Magnetit (Mineral)
Verhältnisformel Fe3O4 CAS-Nummer 1309-38-2 Kurzbeschreibung tiefschwarzes, ferromagnetisches Pulver[1]
Eigenschaften Molare Masse 231,54 g·mol−1 Aggregatzustand fest
Dichte 5,2 g·cm−3[2]
Schmelzpunkt 1538 °C[2]
Löslichkeit unlöslich in Wasser[2]
Sicherheitshinweise EU-Gefahrstoffkennzeichnung [2] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: keine S-Sätze MAK 1,5 mg·m−3 (Aerosolanteil)[2]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Eisen(II,III)-oxid ist ein Oxid des Eisens, das sowohl zwei- wie dreiwertiges Eisen enthält. Es hat die chemische Formel FeO · Fe2O3 bzw. Fe3O4 und wird deshalb auch als Trieisentetraoxid bezeichnet. In der Natur findet es sich als Magnetit. Der Schmelzpunkt liegt bei 1538 °C.
Inhaltsverzeichnis
Darstellung
Aus Eisen und Sauerstoff bei sehr hohen Temperaturen:
Aus Eisen und Wasserdampf bei Temperaturen unterhalb 560 °C
Aus Eisen(III)-oxid bei Temperaturen oberhalb 1200 °C
Als Eisenhammerschlag oder Zunder bezeichnete man früher die beim Schmieden von glühendem Eisen abspringenden Eisenteilchen, die an der Luft sofort zu Fe3O4 oxidierten.
Sinter ist eine weitere Bezeichnung für die Eisenoxide, die beim Strangguß bei der Herstellung von Stahlbrammen anfallen. Bei diesem Verfahren wird der flüssige heiße Stahl von Temperaturen › 1536 °C auf weniger als 200 °C mit Spritzwasser abgekühlt. Durch den Kontakt des heißen Stahls mit Wasser bilden sich auf der Oberfläche der Brammen Eisenoxide, die neben Eisen(III)-oxid einen hohen Anteil an Magnetit enthalten.
Eigenschaften
Schwarze, temperaturbeständige, ferrimagnetische Substanz mit Spinellstruktur. Unlöslich in Wasser, Säuren und Laugen, löslich jedoch in Flusssäure.
Verwendung
Als Pigment Eisenoxid-Schwarz für temperaturbeständige, schwarze Einfärbungen. Als Magnetpigment für Ton- und Videobänder.
Eine der wichtigsten Anwendungen ist die als preiswerter Katalysator mit hoher Lebensdauer im Haber-Bosch-Verfahren zur Synthese von Ammoniak. Magnetit dient weiterhin als Katalysatorkomponente bei der Dehydrierung von Ethylbenzen zu Styrol.
Einzelnachweise
- ↑ Helmut Sitzmann in:Römpp Online - Version 3.5, 2009, Georg Thieme Verlag, Stuttgart.
- ↑ a b c d e Eintrag zu Eisen(II,III)-oxid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 18. Januar 2008 (JavaScript erforderlich)
Literatur
- Holleman-Wiberg, Lehrbuch der anorganischen Chemie (2007)
Kategorien:- Eisenverbindung
- Oxid
- Pharmazeutischer Hilfsstoff
Wikimedia Foundation.




