- Kobalt(II)-oxid
-
Kristallstruktur 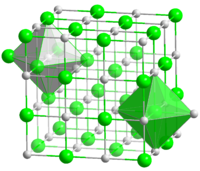
__ Co2+ __ O2- Allgemeines Name Cobalt(II)-oxid Andere Namen - Cobaltmonoxid
- Kobalt(II)-oxid
Verhältnisformel CoO CAS-Nummer 1307-96-6 Kurzbeschreibung grünes Pulver Eigenschaften Molare Masse 74,93 g·mol–1[1] Aggregatzustand fest
Dichte 6,45 g·cm–3[1]
Schmelzpunkt 1795 °C[1]
Löslichkeit fast unlöslich in Wasser (3,13 mg/l[1])
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 

Gesundheits-
schädlichUmwelt-
gefährlich(Xn) (N) R- und S-Sätze R: 22-43-50/53 S: (2)-24-37-60-61 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Cobalt(II)-oxid ist eines von mehreren Oxiden des chemischen Elementes Cobalt. Es ist ein olivgrünes, in Wasser unlösliches Salz.
Inhaltsverzeichnis
Gewinnung und Darstellung
Cobalt(II)-oxid entsteht, wenn elementares Cobalt an der Luft oder Cobalt(II)-nitrat, Cobalt(II)-hydroxid oder Cobalt(II)-carbonat unter Luftabschluss erhitzt werden.
Eigenschaften
Die Verbindung kristallisiert in der Natriumchlorid-Struktur. Meist kommt (ähnlich wie bei Eisen(II)-oxid FeO) ein leichter Cobalt-Unterschuss vor. Trocken ist Cobaltoxid beständig, feucht kann es leicht zu Cobaltoxidhydroxid CoO(OH) oxidiert werden. Unterhalb von 16 °C ist die Verbindung antiferromagnetisch [3].
Wird es an der Luft auf 400-500 °C erhitzt, bildet sich Cobalt(II,III)-oxid.
Verwendung
Cobalt(II)-oxid wird als Rohstoff für die Herstellung von Pigmenten in der Keramikindustrie (Thénards Blau) verwendet.
Quellen
- ↑ a b c d Eintrag zu Cobalt(II)-oxid in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 13.06.2007 (JavaScript erforderlich)
- ↑ Eintrag zu CAS-Nr. 1307-96-6 im European chemical Substances Information System ESIS
- ↑ P.S. Silinsky and M.S. Seehra, Phys. Ref. B 24, 419 (1981) http://prola.aps.org/abstract/PRB/v24/i1/p419_1
Literatur
- Holleman-Wiberg: Lehrbuch der Anorganischen Chemie 102. Auflage, de Gruyter, Berlin, 2007, ISBN 978-3-11-017770-1.
- N.N. Greenwood, A. Earnshaw: Chemie der Elemente, VCH Verlagsgesellschaft, 1. Auflage 1988, ISBN 3-527-26169-9
Wikimedia Foundation.
