- M-Toluylsäure
-
Toluylsäuren Name 2-Toluylsäure 3-Toluylsäure 4-Toluylsäure Andere Namen o-Toluylsäure
2-Methylbenzoesäurem-Toluylsäure
3-Methylbenzoesäurep-Toluylsäure
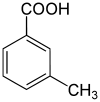
4-MethylbenzoesäureStrukturformel 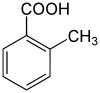

CAS-Nummer 118-90-1 99-04-7 99-94-5 PubChem 8373 7418 7470 Summenformel C8H8O2 Molare Masse 136,15 g·mol−1 Aggregatzustand fest Kurzbeschreibung gelbliche Schuppen weißes kristallines Pulver Schmelzpunkt 101–104 °C[1] 110–111 °C[2] 180–183 °C[3] Siedepunkt 260 °C[1] 263 °C[2] 274 °C[3] pKs-Wert[4] 3,91 4,27 4,37 Löslichkeit 1,2 g·l−1[1] 1 g·l−1[2] 0,3 g·l−1[3] Gefahrstoff-
kennzeichnung
[1][2][3]
Gesundheits-
schädlich(Xn) R-Sätze 22-36/37/38 22-36/37/38 22-36 S-Sätze 26-37/39 26-36/37 keine S-Sätze Die Toluylsäuren (oder Methylbenzoesäuren) bilden eine Stoffgruppe, die sich sowohl von der Benzoesäure als auch vom Toluol ableitet. Die Struktur besteht aus einem Benzolring mit angefügter Carboxyl- (–COOH) und Methylgruppe (–CH3). In erster Linie kann man sie als methylsubstituierte Benzoesäuren ansehen. Durch deren unterschiedliche Anordnung ergeben sich drei Konstitutionsisomere.
Eigenschaften
Die Toluylsäuren sind weiße bis gelbliche Feststoffe. Die Schmelzpunkte unterscheiden sich deutlich. Die 4-Toluylsäure, die die höchste Symmetrie aufweist, besitzt den höchsten Schmelzpunkt.
Darstellung
Aus den Xylolen erhält man die Toluylsäuren durch Sauerstoff (z. B. in Gegenwart von Cobaltstearat als Katalysator); es wird nur eine Methylgruppe selektiv oxidiert. Verwendet man jedoch stärkere Oxidationsmittel wie Kaliumpermanganat oder Chromschwefelsäure, so werden beide Methylgruppen oxidiert und somit o-Xylol in Phthalsäure, m-Xylol in Isophthalsäure und p-Xylol in Terephthalsäure überführt.
Einzelnachweise
- ↑ a b c d Eintrag zu CAS-Nr. 118-90-1 in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 13. April 2009 (JavaScript erforderlich).
- ↑ a b c d Eintrag zu CAS-Nr. 99-04-7 in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 13. April 2009 (JavaScript erforderlich).
- ↑ a b c d Eintrag zu CAS-Nr. 99-94-5 in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 13. April 2009 (JavaScript erforderlich).
- ↑ CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
Wikimedia Foundation.
