- Benzoesäure
-
Strukturformel 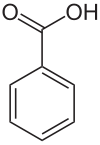
Allgemeines Name IUPAC: Benzoesäure (gebräuchlich) Andere Namen - Phenylameisensäure
- Benzolcarbonsäure
- Benzencarbonsäure (IUPAC)
- Phenylcarbonsäure (systematisch)
- Carboxybenzen
- Monophenylmethansäure
Summenformel C7H6O2 CAS-Nummer 65-85-0 PubChem 243 Kurzbeschreibung farbloser Feststoff mit charakteristischem Geruch[1]
Eigenschaften Molare Masse 122,12 g·mol−1 Aggregatzustand fest
Dichte 1,27 g·cm−3[1]
Schmelzpunkt Siedepunkt 250 °C[1]
Dampfdruck pKs-Wert 4,2[3]
Löslichkeit Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [1] 
Achtung
H- und P-Sätze H: 302-319 EUH: keine EUH-Sätze P: 305+351+338 [1] EU-Gefahrstoffkennzeichnung [1] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 22-36 S: 24 MAK nicht festgelegt[1]
LD50 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Benzoesäure (gesprochen: Benzo-e-säure) ist eine aromatische Carbonsäure. Sie besteht aus einem Phenylrest mit einer Carboxygruppe. Die Salze und Ester der Benzoesäure werden Benzoate genannt.
Inhaltsverzeichnis
Eigenschaften
Benzoesäure bildet farblose, glänzende Blättchen oder nadelförmige Kristalle, die in kaltem Wasser nur wenig, in warmem Wasser dagegen besser löslich sind. Über 370 °C zersetzt sich Benzoesäure langsam in Benzol und Kohlenstoffdioxid (CO2). Benzoesäure hat einen intensiven Geruch und ist gut brennbar.
Vorkommen
Als ein Hauptbestandteil des Harzes Benzoe ist Benzoesäure in vielen Weihrauchmischungen enthalten. Benzoe ist das Harz zweier Baumarten (Siam-Benzoe und Sumatra-Benzoe), die in Südostasien beheimatet sind. Daneben findet sich Benzoesäure auch in Früchten, zum Beispiel Pflaumen, Heidel- und Preiselbeeren.
Darstellung
Technisch erfolgt die Herstellung durch eine Oxidation von Toluol mit Braunstein und Schwefelsäure in Gegenwart von Mangannaphthenat, oder durch die Reaktion mit Kaliumpermanganat. Industriell wird heute Toluol mit Sauerstoff in der Gasphase in Gegenwart von Katalysatoren wie z. B. Vanadiumpentoxid oxidiert.
Weiterhin kann Benzoesäure über eine Grignard-Reaktion ausgehend von Brombenzol hergestellt werden. Das Brombenzol reagiert mit Magnesium zu Phenylmagnesiumbromid, welches mit Kohlenstoffdioxid zu C6H5COOMgBr und schließlich durch Zugabe einer Salzsäurelösung zu Benzoesäure reagiert.
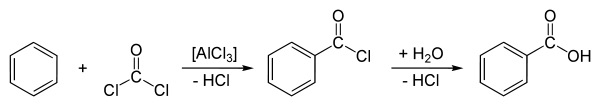
Schließlich kann Benzoesäure durch Carboxylierung von Benzol mittels Phosgen und Aluminiumtrichlorid (AlCl3) als Katalysator dargestellt werden. Diese Reaktion besteht aus einer Friedel-Crafts-Acylierung und anschließender Hydrolyse des Zwischenprodukts Benzoylchlorid:
Verwendung
Benzoesäure wird bei der Herstellung von Benzoesäureestern (z. B. Benzoesäureethylester) gebraucht, die in der Parfümindustrie als Biozide Anwendung finden. Außerdem wird Benzoesäure für Weichmacher, bei der Darstellung von Benzoylverbindungen, wie beispielsweise Benzoylchlorid und Dibenzoylperoxid, verwendet.
In der Lebensmittelindustrie wird Benzoesäure (E 210) als Konservierungsmittel vor allem bei sauer eingelegten Lebensmitteln eingesetzt. Wegen besserer Löslichkeit ist eher die Verwendung der Salze üblich: Natriumbenzoat (E 211), Kaliumbenzoat (E 212), Calciumbenzoat (E 213).[5]
Benzoesäure wird häufig in haltbaren Nahrungsmitteln wie z. B. in Ketchup, Wurst, Senf und anderen Soßen, Margarine, Fischsalaten und vielen anderen Produkten als Konservierungsstoff verwendet. Die bakteriostatische und fungistatische Wirkung beruht auf dem Hemmeffekt gegenüber Enzymen, die reaktive Sauerstoffspezies abbauen (Katalase und Peroxidase), wodurch eine Wasserstoffperoxid-Ansammlung in den Zellen der Mikroorganismen erzeugt wird. Diese führt letztlich zu deren Absterben.
Benzoesäure kann pseudoallergische Reaktionen auslösen.[1] Die Verbindung wird im Zusammenhang mit Konzentrationsproblemen und Hyperaktivität bei Kindern diskutiert.[6] Das BfR wies auf eine mögliche Bildung von geringen Mengen giftigen Benzols aus Benzoesäure in Verbindung mit Ascorbinsäure (Vitamin C) hin. Ob überhaupt und in welchem Ausmaß Benzol in einer Lebensmittelmatrix gebildet werden kann ist noch nicht untersucht.[7]
In der Umweltbeobachtung werden Bodenfallen mit gesättigter Benzoesäurelösung gefüllt, um erfasste Lebewesen wie Insekten oder Schnecken zu töten und bis zur nächsten Leerung zu fixieren.
Benzoesäure ist eine Urtitersubstanz nach Arzneibuch.
Einzelnachweise
- ↑ a b c d e f g h i j Eintrag zu Benzoesäure in der GESTIS-Stoffdatenbank des IFA, abgerufen am 22. August 2007 (JavaScript erforderlich).
- ↑ Datenblatt Benzoesäure bei Merck, abgerufen am 28. Dezember 2010.
- ↑ Charles E. Mortimer: Chemie – Das Basiswissen der Chemie. Thieme 2003, ISBN 3-13-484308-0.
- ↑ Benzoesäure bei ChemIDplus.
- ↑ ZZulV: Anlage 5 (zu § 5 Abs. 1 und § 7) – Zusatzstoffe, die für Lebensmittel zur Konservierung oder als Antioxidationsmittel zugelassen sind.
- ↑ Artikel auf Welt-Online.
- ↑ Stellungnahme Nr. 013/2006 des BfR vom 1. Dezember 2005: Hinweise auf eine mögliche Bildung von Benzol aus Benzoesäure in Lebensmitteln.
Weblinks
 Wiktionary: Benzoesäure – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen
Wiktionary: Benzoesäure – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen- Umfangreiche Informationen der Verbraucherinitiative zum Thema Benzoesäure
- Das chemisch konservierte Klima – Radiofeulieton Mahlzeit
Kategorien:- Gesundheitsschädlicher Stoff
- Benzolcarbonsäure
- Lebensmittelkonservierungsstoff
- Pharmazeutischer Hilfsstoff
Wikimedia Foundation.