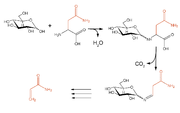
- Maillardreaktion
-
Die Maillard-Reaktion (benannt nach dem Chemiker Louis Camille Maillard) ist eine so genannte nicht-enzymatische Bräunungsreaktion. Hierbei werden Aminosäuren und reduzierende Zucker unter Hitzeeinwirkung zu neuen Verbindungen umgewandelt. Sie ist nicht zu verwechseln mit dem Karamellisieren, jedoch können beide Reaktionen gemeinsam auftreten.
Die Maillard-Reaktion ist von Bedeutung für das Kochen und die Lebensmittelindustrie, denn die braunen, Melanoidine genannten Endprodukte sind geschmackintensiv und für das typische Aroma und die Färbung von eiweißreichem Geröstetem, Gebackenem und Gebratenem verantwortlich. Die Reaktion verzögert auch den Verderb, da die Melanoide/Melanoidine wie das Pronyl-Lysin Luftsauerstoff binden. Forscher aus Madrid und aus Japan ermittelten außerdem eine schwach antibakterielle (keimhemmende) Wirkung.[1] Die Maillard-Reaktion kann aber auch unerwünschte Geschmacksveränderungen beim Sterilisieren von beispielsweise Fleisch oder Milchprodukten hervorrufen und selbst ohne Hitzeeinwirkung bei langer Lagerung proteinhaltiger Lebensmittel auftreten.
In der mehrstufigen Reaktion wird ab etwa 140 °C zuerst unter Abspaltung von Wasser eine Aminosäure mit einem Zucker verbunden. Es entsteht eine Schiffsche Base, die sich in mehreren Schritten zu einer cyclischen Verbindung umlagert. Es entstehen hochreaktive Alpha-Dicarbonylverbindungen und daraus viele weitere, teilweise farbige Verbindungen.
Die Anzahl möglicher Reaktionsprodukte ist sehr hoch, viele Verbindungen sind noch unbekannt. Oft entstehen heterocyclische Verbindungen.
Beispiel einer unerwünschten Maillard-Reaktion ist die bei großer Hitze stattfindende Bildung des Karzinogens Acrylamid aus der Aminosäure Asparagin (etwa in Kartoffel- und Getreideprodukten). Unerwünschte Maillard-Reaktionen führen zu zahlreichen weiteren, potentiell mutagen oder/und karzinogen wirkenden Verbindungen. Die Zusammenhänge sind teilweise noch zu klären.
Die Maillard-Reaktion spielt außerdem eine Rolle in gewissen Alterungsprozessen im menschlichen Körper und beim Diabetes mellitus.[2][3] Hierbei führen oxidative Reaktionen zu Schädigungen am Körpergewebe. Im Sommer 2004 wurden auf einer Hamburger Konferenz jedoch überraschende Zwischenergebnisse einer EU-Studie (seit 1998) vorgestellt, welche auch antioxidative Wirkungen der Maillard-Produkte belegen. Eine Gruppe italienischer Wissenschaftler um Vincenzo Fogliano von der Universität Neapel entdeckte darüber hinaus, dass Melanoidine einer Entstehung von Metastasen entgegenwirken können.[4][5]
Die im Labor erzeugten Maillard-Produkte blockieren bestimmte Proteine, die Lektine[6], die den Zusammenhalt von Krebszellen bewirken und damit die Metastasenbildung beschleunigen. Andererseits weisen Patienten mit Diabetes (s. o.) bzw. Nierenfunktionsstörungen einen erhöhten Melanoidinspiegel auf. Hier sind die Zusammenhänge letztlich noch ungeklärt.
Quellen
- ↑ Shigeru Hiramoto et al.: Melanoidin, a food protein-derived advanced maillard reaction product, suppresses Helicobacter pylori in vitro and in vivo, Helicobacter. 2004 Oct ;9 (5):429–35 15361082
- ↑ Ralf Liedke: Bildung von Dicarbonylverbindungen beim Abbau von Amadori-Umlagerungsprodukten. Inaugural-Dissertation, 1999, S. 1-16.
- ↑ E. Schleicher: Die Bedeutung der Maillard-Reaktion in der menschlichen Physiologie, Zeitschrift für Ernährungswissenschaft, Vol. 30, Number 1, 1991
- ↑ Vincenzo Fogliano: Biochimica degli alimenti
- ↑ Encarta: Caffé e antiossidanti: i segreti per una buona salute nascosti in una tazzina?
- ↑ Frankfurter Allgemeine Zeitung: Ist die Bratwurst gesünder als ihr Ruf?, 29. September 2004
Wikimedia Foundation.