- Mangan(VII)-oxid
-
Strukturformel 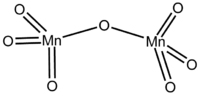
Allgemeines Name Mangan(VII)-oxid Andere Namen Dimanganheptoxid
Summenformel Mn2O7 CAS-Nummer 12057-92-0 PubChem 13879826 Kurzbeschreibung ölige, grünlichbraune Flüssigkeit[1]
Eigenschaften Molare Masse 221,87 g·mol–1 Aggregatzustand flüssig
Dichte 2,40 g·cm–3[1]
Schmelzpunkt Siedepunkt Zersetzung ab 40 °C[1]
Löslichkeit Zersetzung bei Kontakt mit Wasser in Permangansäure[2]
Sicherheitshinweise EU-Gefahrstoffkennzeichnung [3] keine Einstufung verfügbar R- und S-Sätze R: siehe oben S: siehe oben Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Mangan(VII)-oxid ist eine chemische Verbindung mit der Summenformel Mn2O7. Die ölige Flüssigkeit ist hochreaktiv, da sie ein starkes Oxidationsmittel ist. Die erste Beschreibung erfolgte 1860.[4]
Inhaltsverzeichnis
Gewinnung und Darstellung
Mangan(VII)-oxid wird durch die Reaktion von Schwefelsäure mit Kaliumpermanganat gewonnen.
Eigenschaften
Bei niedrigen Temperaturen liegt die Verbindung als kristalliner Feststoff vor, der grünes Licht reflektiert und im Durchlicht rot aussieht. Die Verbindung besteht aus einem Paar Tetraeder, die über ein Sauerstoffatom verbunden sind, was mit der Strukturformel O3Mn–O–MnO3 beschrieben werden kann. Die außenliegenden Mn–O–Bindungen haben eine Länge von 158,5 pm, die zentrale Bindung von 177 pm. Die zentrale Mn–O–Mn-Bindung hat einen Winkel von 120,7°.[5] Diese Eigenschaften ähneln Pyrosulfaten, Pyrophosphaten, Dichromaten und anderen R2O7–Verbindungen (wobei R für Chlor oder Metalle wie Technetium oder Rhenium[6] steht).
Sicherheitshinweise
Mangan(VII)-oxid ist eine hochreaktive Verbindung. Sie zersetzt sich ab 40 °C und explodiert bei höheren Temperaturen, wobei die Explosion auch durch Schlag oder Verunreinigungen ausgelöst werden kann. Es entstehen dabei Mangan(IV)-oxid (Braunstein), Sauerstoff sowie geringe Mengen an Ozon, was der Verbindung einen starken Geruch verleiht. Sie verkohlt organische Stoffe, wie etwa Holz, sofort. Mit Aceton oder anderen Lösungsmitteln erfolgt Selbstentzündung.
Einzelnachweise
- ↑ a b c d Eintrag zu Mangan(VII)-oxid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 30. Mai 2008 (JavaScript erforderlich).
- ↑ http://www.uni-bayreuth.de/departments/ddchemie/umat/mangan/oxmangan.htm
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ H. Aschoff, Ann. Phys. Chem., 1860, 2, 111, S. 217–224.
- ↑ A. Simon, R. Dronskowski, B. Krebs, B. Hettich: Die Kristallstruktur von Mn2O7. In: Angew. Chem., 1987, 99, S. 160–161.
- ↑ B. Krebs, A. Mueller, H. H. Beyer: The Crystal Structure of Rhenium(VII) Oxide. In: Inorg. Chem., 1969, 8, S. 436–443.
Wikimedia Foundation.


