- Simmons-Smith-Reaktion
-
Die Simmons-Smith-Reaktion ist eine chemische Reaktion, die in der Organischen Chemie zur Synthese von Derivaten des Cyclopropans benutzt wird. Es handelt sich um die Addition eines Zinkcarbenoids an eine Doppelbindung. Sie ist benannt nach ihren Entwicklern Howard Ensign Simmons Jr. und R. D. Smith.[1][2]
Inhaltsverzeichnis
Mechanismus
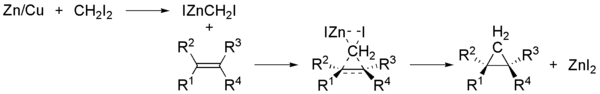
Zur Simmons-Smith-Reaktion wird zunächst aus Diiodmethan und überschüssigem aktivierten Zink ein Zinkcarben erzeugt. Das aktivierte Zink ist durch Verwendung des Zink-Kupfer-Paares erhältlich. Das Carbenoid addiert dann in einer konzertierten Reaktion an die Doppelbindung des eingesetzten Alkens.
Die Simmons-Smith-Reaktion verläuft stereospezifisch. Das bedeutet, dass bei Verwendung von cis-Alkenen cis-Cyclopropanderivate erhalten werden und bei Verwendung eines trans-Alkens die entsprechenden trans-Derivate. Anstelle das Zink-Kupfer-Paares kann auch Diethylzink als Zinkquelle verwendet werden.[3][4]
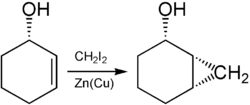
Enthält das verwendete Alken an einem Chiralitätszentrum eine funktionelle Gruppe, die mit Zinkionen eine koordinative Bindung eingehen kann, so kann hierüber eine Stereoinformation induziert werden, die zur bevorzugten Bildung eines Stereoisomers führt.[5]
Durch sterisch anspruchsvolle Reste kann der Angriff von dieser Seite gehindert werden und die Cyclopropanierung findet bevorzugt von der anderen Seite statt.[6]
Asymmetrische Simmons-Smith-Reaktion
Durch Verwendung chiraler Liganden kann die Simmons-Smith-Reaktion auch enantioselektiv geführt werden. Dies gelang erstmals 1992 unter Verwendung chiraler Disulfonamid-Liganden.[7]
Literatur
T. Laue, A. Plagens: Namen- und Schlagwort-Reaktionen. 4. Auflage, Teubner, Wiesbaden 2004, ISBN 3-519-33526-3.
Einzelnachweise
- ↑ H. E. Simmons Jr., R. D. Smith: A new Synthesis of Cyclopropanes from Olefins, in: J. Am. Chem. Soc. 1958, 80, 5323–5324.
- ↑ H. E. Simmons, R. D. Smith: A New Synthesis of Cyclopropanes, in: J. Am. Chem. Soc. 1959, 81, 4256–4264.
- ↑ A. B. Charette, H. Lebel: (2S,3S)-(+)-(3-Phenylcyclopropyl)methanol. In: Org. Synth. 2004, 10, 613.
- ↑ Y. Ito: One-Carbon Ring Expansion of Cycloalkanones to Conjugated Cycloalkenones: 2-Cyclohepten-1-one. In: Org. Synth., 1988, 6, 327.
- ↑ Grieco et al. J. Org. Chem. 1977, 42, 4113.
- ↑ H. E. Simmons, Org. React. 1973, 20, 1.
- ↑ H. Takahashi, M. Yoshioka, M. Ohno, S. Kobayashi: A catalytic enantioselective reaction using a C2-symmetric disulfonamide as a chiral ligand: cyclopropanation of allylic alcohols by the Et2Zn-CH2I2-disulfonamide system, Tetrahedron Lett. 1992, 33, 2575–2578.
Wikimedia Foundation.