- Upjohn-Dihydroxylierung
-
Die Dihydroxylierung bezeichnet eine Chemische Reaktion, mit der an die Doppelbindung eines Alkens zwei vicinalen Hydroxygruppen addiert werden. Da sich die Oxidationszahl der Kohlenstoffatome dabei erhöht, handelt es sich um eine Oxidationsreaktion. In der Organischen Chemie sind Dihydroxylierungsreaktionen weit verbreitet, die bekannteste ist die sogenannte Upjohn-Dihydroxylierung mit katalytisch eingesetztem Osmiumtetroxid (OsO4) und N-Methylmorpholin-N-oxid (NMO). Für die nach ihrem Entdecker Barry Sharpless benannte stereoselektive Sharpless-Dihydroxylierung wurde 2001 der Nobelpreis für Chemie vergeben.
Inhaltsverzeichnis
Reagenzien
Die für die Reaktion benötigten Oxidationsmittel sind in der Regel Oxide von Übergangsmetallen wie Osmiumtetroxid (OsO4), Permanganat (MnO4–) oder Rutheniumtetroxid (RuO4). Während Permanganat preiswert genug ist, um es auch stöchiometrisch, also im Verhältnis 1:1 mit dem Ausgangsstoff (Edukt), einzusetzen, werden Osmium- und Rutheniumtetroxid häufig nur in katalytischen Mengen eingesetzt. Um dies zu ermöglichen, wird das Reaktionsprodukt, die Osmium(VI)- bzw. Ruthenium(VI)-säure, mit Hilfe eines Cooxidans wieder zum Tetroxid oxidiert und kann somit eine weiteres Eduktmolekül umsetzen. Als Cooxidans wird für das Oxidationsmittel OsO4 N-Methylmorpholin-N-oxid (NMO) und für RuO4 Natriumperiodat (NaIO4) eingesetzt.
Zur stereoselektiven Dihydroxylierung wird ein spezielles Gemisch aus Oxidationsmitteln und geeigneten Katalysatoren eingesetzt, die im entsprechenden Abschnitt detailliert erläutert werden.
Reaktionsmechanismus
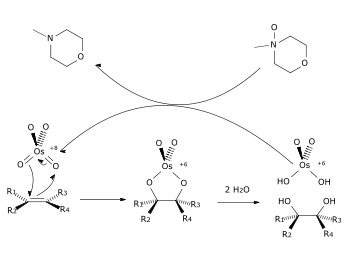
Der Mechanismus für die Dihydroxylierung ist für Osmiumtetroxid als Oxidationsreagenz umfangreich untersucht und bestätigt. Es wird angenommen, dass Permanganat und Rutheniumtetroxid analog reagieren. Die Reaktion beginnt mit einer 1,3-dipolaren Cycloaddition des Oxidationsmittels an die Doppelbindung. Der entstandene fünfgliedrige Ring ist ein Diester der Osmium(VI)-säure, welcher in Anwesenheit von Wasser gespalten (hydrolysiert) wird und das Endprodukt freisetzt. Aufgrund des Fünfringintermediats entsteht ausschließlich das cis-Additionsprodukt. Die entstandene Osmium(VI)-säure OsO2(OH)2 wird anschließend durch NMO wieder in das achtwertige Osmiumtetroxid überführt.
Je nach Art des Oxidationsmittel unterscheidet sich der Verlauf der Reaktion: RuO4 ist als einziges in der Lage, auch Doppelbindungen in einem Aromaten selektiv zu dihydroxylieren. OsO4 greift diese Doppelbindungen nicht an, bei Einsatz von Permanganat hingegen wird das Produkt direkt weiter umgesetzt und unterläuft eine Oxidative Spaltung. Diese Folgereaktion kann unter bestimmten Reaktionsbedingungen auch bei der Dihydroxylierung von Alkenen mit Permanganat auftreten.
Ligandenbeschleunigung
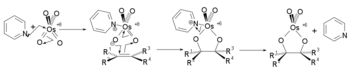
Die Reaktion kann durch Zugabe einer Base wie Pyridin zusätzlich beschleunigt werden. Hierbei koordiniert das freie Elektronenpaar der Base am Metallzentrum und erzeugt so eine negative Ladung an den Sauerstoffliganden. Dies beschleunigt die Cycloaddition an die Doppelbindung und damit den gesamten Ablauf der Reaktion. Da die Base jedoch nicht direkt in die Reaktion eingreift, sondern als zusätzlicher Ligand am Katalysator wirkt, spricht man von einer Ligandenbeschleunigung.
Stereoselektive Dihydroxylierung
Die von Sharpless entwickelte stereoselektive Dihydroxylierung, auch asymmetrische Dihydroxylierung (abk. AD) genannt, war Teil der Begründung für die Vergabe des Nobelpreises 2001 und ist derzeit eine der bekanntesten stereoselektiven Synthesemethoden. Erwähnenswert ist die hohe Enantioselektivität, die bei Einsatz der unterschiedlichsten Edukte erreicht wird, sowie das diese Selektivität auf einem katalytischen System beruht, dem eine Ligandenbeschleunigung zu Grunde liegt.
Reagenzien
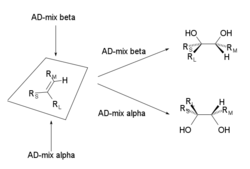
Neben den bereits erwähnten Oxidationsmitteln und dem Cooxidans werden der Reaktion zusätzlich eine Reihe von chiralen Stoffen, meist Dihydrochinin- oder Dihydrochinidinderivate[1], zugesetzt. Die gesamte Mischung wird als AD-mix bezeichnet.
Literatur
- R. Brückner, Reaktionsmechanismen, 2. Aufl., Spektrum Verlag, Heidelberg/Berlin 2003, S. 750–758, ISBN 3-8274-1189-0.
Einzelnachweise
- ↑ P. Duoau, R. Epple, A.A. Thomas, V.V. Fokin, K.B. Sharpless, Adv. Synth. Catal. 2002, 344, 421.
Weblinks
Wikimedia Foundation.