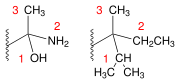
- Cahn-Ingold-Prelog-System
-
Die Cahn-Ingold-Prelog-Konvention (kurz: CIP-Konvention oder RS-System) dient zur eindeutigen Beschreibung der Anordnung der unterschiedlichen Substituenten an Atomen, also der Bestimmung der absoluten Konfiguration der Stereozentren chiraler und insbesondere stereoisomerer Moleküle. Sie wurde 1966 von Robert Sidney Cahn, Christopher Kelk Ingold und dem Schweizer Nobelpreisträger Vladimir Prelog vorgeschlagen[1] und 1982 von Vladimir Prelog und Günter Helmchen überarbeitet.[2]
Inhaltsverzeichnis
Vorgehensweise bei der Bestimmung
Es wird folgendermaßen vorgegangen:
- Zuerst werden die Stereozentren des Moleküls bestimmt. Ein Stereozentrum ist zumeist ein Kohlenstoffatom, das vier verschiedene Substituenten trägt. Bei anderen Atomen, wie z. B. Phosphor, Schwefel (siehe Omeprazol), kann auch ein freies Elektronenpaar als Substituent gelten. Man markiert die Stereozentren in der Strukturformel durch Sternchen.
- Dann wird die so genannte Zählrichtung oder Drehrichtung der Struktur am zu bestimmenden Stereozentrum (nicht identisch mit der optischen Drehrichtung!) durch Ordnung der Substituenten bestimmt:
- Zuerst untersucht man die vier Atome, die direkt an das Stereozentrum gebunden sind. Die Atome erhalten Prioritätsnummern. Das Atom mit der höchsten Ordnungszahl im Periodensystem erhält die Ziffer 1, das mit der zweithöchsten Ordnungszahl die Ziffer 2 und so weiter. Freie Elektronenpaare haben dabei eine geringere Priorität als das Element mit der niedrigsten Ordnungszahl, Wasserstoff.
- Bei gleicher Ordnungszahl hat der Substituent mit der höheren Masse die höhere Priorität; dies spielt beim Einbau von z. B. Deuterium eine Rolle (D>H)
- Bei gleichen Ordnungszahlen und gleicher Masse hat der Substituent die höhere Priorität (kleinere Ziffer), der an ein anderes Atom (Zweitatom) mit der höchsten Ordnungszahl gebunden ist; genauer gilt, dass in diesem Falle die sogenannte 2. Sphäre (eine Menge von Atomen) des einen Substituenten mit der 2. Sphäre des anderen Substituenten verglichen wird. Da nun eine Menge von Atomen mit einer Menge von anderen Atomen verglichen wird, sind die Vergleichsregeln etwas involvierter:
- Doppel- und Dreifachbindungen werden so behandelt, als ob das jeweilige Atom bzw. die jeweilige Gruppe doppelt bzw. dreifach vorhanden wäre.
- Auf jeder Seite werden die Atome nach Ordnungs- und (sekundär) Massenzahl sortiert, und dann, beginnend mit den höchsten, verglichen, bis es einen Unterschied gibt.
- Falls nötig muss das Verfahren rekursiv jeweils am Atom mit der höchsten Priorität wiederholt werden.
- Ist man an einem Molekülende angelangt, und hat immer noch keinen Unterschied gefunden, dann geht man jeweils eine Bindung zurück und wiederholt das Verfahren mit dem nächstpriorisierten Atom.
- Für stereochemische Unterschiede gelten dabei zusätzlich die Regeln Z vor E, cis vor trans und R vor S.
- Bei gleichen Ordnungszahlen und gleicher Masse hat der Substituent die höhere Priorität (kleinere Ziffer), der an ein anderes Atom (Zweitatom) mit der höchsten Ordnungszahl gebunden ist; genauer gilt, dass in diesem Falle die sogenannte 2. Sphäre (eine Menge von Atomen) des einen Substituenten mit der 2. Sphäre des anderen Substituenten verglichen wird. Da nun eine Menge von Atomen mit einer Menge von anderen Atomen verglichen wird, sind die Vergleichsregeln etwas involvierter:
- Bei gleicher Ordnungszahl hat der Substituent mit der höheren Masse die höhere Priorität; dies spielt beim Einbau von z. B. Deuterium eine Rolle (D>H)
- Der Substituent mit der niedrigster Priorität 4 wird unter die Bildebene gestellt. Anschließend zählt man kreisförmig um das aktive Zentrum vom Substituenten mit der Priorität 1 bis zur Priorität 3. Läuft diese Kreisbewegung rechtsherum, also im Uhrzeigersinn, so liegt eine (R)-Konfiguration vor, läuft sie linksherum (gegen den Uhrzeigersinn), so liegt eine (S)-Konfiguration vor. Dieser Vorgang wird für jedes Stereozentrum wiederholt. R ist die Abkürzung von lateinisch rectus (rechts) und S von lateinisch sinister (links).
- Zuerst untersucht man die vier Atome, die direkt an das Stereozentrum gebunden sind. Die Atome erhalten Prioritätsnummern. Das Atom mit der höchsten Ordnungszahl im Periodensystem erhält die Ziffer 1, das mit der zweithöchsten Ordnungszahl die Ziffer 2 und so weiter. Freie Elektronenpaare haben dabei eine geringere Priorität als das Element mit der niedrigsten Ordnungszahl, Wasserstoff.
Einige Beispiele für die Priorität der Substituenten sind hier in abfallender Priorität dargestellt:
-I > -Cl > -S-CH3 > -SH > -F > -O-CH3 > -OH > -N3 > -N (CH3)2 > -NH-C6H5 > -NH2 > -COOH > -CON2H >
> -CONH2 > -CHO > -CH2OH > -CD3 > -CD2H > -CDH2 > -CH3 > -D > -H > freies Elektronenpaar
Die CIP-Regeln können auch zur eindeutigen Bestimmung der Konfiguration von Molekülen mit Chiralitätsachsen, Chiralitätsebenen oder helikalen Strukturen verwendet werden.
Literatur
- ↑ R.S. Cahn, C.K. Ingold & V. Prelog (1966): Spezifikation der molekularen Chiralität. In: Angew. Chem. Bd. 78, S. 413–447. Abstract
- ↑ V. Prelog & G. Helmchen (1982): Grundlagen des CIP-Systems und Vorschläge für eine Revision. In: Angew. Chem. Bd. 94, S. 614-631. Abstract
Weblinks
Siehe auch
Wikimedia Foundation.