- Caesiumacetat
-
Strukturformel 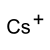
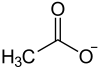
Allgemeines Name Caesiumacetat Andere Namen Caesiumethanoat (nach IUPAC)
Summenformel C2H3Cs CAS-Nummer 3396-11-0 PubChem 5152919 Kurzbeschreibung Eigenschaften Molare Masse 191,96 g·mol−1 Aggregatzustand fest
Schmelzpunkt Löslichkeit gut in Wasser [2]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [3] keine GHS-Piktogramme H- und P-Sätze H: keine H-Sätze EUH: keine EUH-Sätze P: keine P-Sätze EU-Gefahrstoffkennzeichnung [3] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: 22-24/25 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Caesiumacetat ist das Caesiumsalz der Essigsäure mit der Summenformel CH3COOCs.
Inhaltsverzeichnis
Gewinnung und Darstellung
Caesiumacetat kann durch Salzbildungsreaktion aus Caesiumhydroxid und Essigsäure hergestellt werden.
Ebenso ist die Synthese aus Caesiumcarbonat und Essigsäure unter Entwicklung von Kohlendioxid möglich.
Eigenschaften
Wasserfreies Caesiumacetat kristallisiert im hexagonalen Kristallsystem[4] in der Raumgruppe P6/m mit den Gitterparametern a = 1488,0 pm und c = 397,65 pm. In der Elementarzelle befinden sich sechs Formeleinheiten.[5]
Die thermische Zersetzung von Caesiumacetat ist bei 450 °C abgeschlossen. Als Endprodukt entsteht Caesiumoxid.[6]
Verwendung
Caesiumacetat findet als Reagens bei der Perkin-Reaktion Verwendung, wo es das sonst übliche Natriumacetat ersetzen kann.[7]
Einzelnachweise
- ↑ a b Datenblatt Caesiumacetat bei Acros, abgerufen am 20. Mai 2010.
- ↑ a b MSDS bei Strem Chemicals
- ↑ a b Datenblatt Cesium acetate bei Sigma-Aldrich, abgerufen am 25. Mai 2011.
- ↑ J. Hatibarua, G. S. Parry: "A crystallographic study of the acetates of potassium, rubidium and caesium" in Acta Cryst. 1972, B28, S. 3099. [1]
- ↑ A. Lossin, G. Meyer: "Kristallstruktur von Caesiumacetat, Cs(CH3COO)" in Zeitschrift für anorganische und allgemeine Chemie 1993, 619(8), S. 1462-1464. doi:10.1002/zaac.19936190823
- ↑ U. Meyer, H. Gorzawski, W. F. Hölderich: "Michael addition of ethyl acrylate and acetone over solid bases" in Catalysis Letters 1999, 59, S. 201-206. doi:10.1023/A:1019020504961
- ↑ E. Koepp, F. Vögtle: "Perkin-Synthese mit Cäsiumacetat" in Synthesis 1987, 1987(2), S. 177-179. doi:10.1055/s-1987-27880
Kategorien:- Caesiumverbindung
- Acetat
Wikimedia Foundation.


