- Lanthanchlorid
-
Kristallstruktur 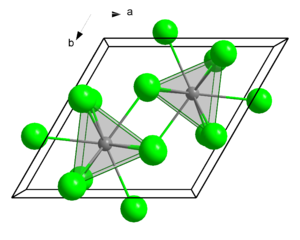
__ La3+ __ Cl− Kristallsystem Raumgruppe 
Gitterkonstanten a = 748,3 pm
c = 436,4 pmKoordinationszahlen La[9], Cl[3]
Allgemeines Name Lanthanchlorid Andere Namen - Lanthan(III)-chlorid
- Lanthantrichlorid
Verhältnisformel LaCl3 CAS-Nummer - 10099-58-8
- 10025-84-0 (Heptahydrat)
- 20211-76-1 (Hydrat)
PubChem 64735 Kurzbeschreibung weißes Pulver[1]
Eigenschaften Molare Masse 245,26 g·mol−1 Aggregatzustand fest
Dichte Schmelzpunkt Siedepunkt 1812 °C[3]
Löslichkeit löslich in Wasser und starken Mineralsäuren[4]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [5] 

Achtung
H- und P-Sätze H: 315-319-335-400 EUH: keine EUH-Sätze P: 261-273-305+351+338 [5] EU-Gefahrstoffkennzeichnung [1] 
Reizend (Xi) R- und S-Sätze R: 36/37/38 S: 26-37/39 LD50 2370 mg·kg−1 (oral Ratte)[1]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Lanthanchlorid ist eine chemische Verbindung aus der Gruppe der Chloride.
Inhaltsverzeichnis
Gewinnung und Darstellung
Lanthanchlorid kann durch Reaktion von Lanthanoxid mit Chlorwasserstoff gewonnen werden.
Eigenschaften
Lanthanchlorid kristallisiert hexagonal in der Raumgruppe P63 / m mit den Gitterparametern a = 748,3 pm , c = 436,4 pm und Z = 2. Das Heptahydrat kristallisiert monoklin mit den Gitterparametern a = 1237 pm, b = 1068 pm, c = 923 pm und einem Winkel von 114,3°.[2] Das Heptahydrat wandelt sich oberhalb von 90 °C in das Anhydrat um.[6]
Verwendung
Lanthanchlorid wird als milde Lewis-Säure für chemische Reaktionen verwendet, die normalerweise saure Bedingungen erfordern, wie zum Beispiel der Umbau von Aldehyden zu Acetalen unter nahezu neutralen Bedingungen. Es dient auch als Katalysator beim Fluid catalytic cracking.[7] Das Heptyhydrat wird in der Medizin als Kalziumkanalblocker eingesetzt[6] und dient weiterhin in der Wasserwirtschaft zur Eindämmung von Algenwachstum durch Bindung von Phosphaten.[8]
Weblinks
- Xiao He, Zhiyong Zhang, Haifeng Zhang, Yuliang Zhao, Zhifang Chai: „Neurotoxicological Evaluation of Long-Term Lanthanum Chloride Exposure in Rats“, in: Toxicological Sciences, 2008, 103 (2), S. 354–361; doi:10.1093/toxsci/kfn046.
- Lanthanum chloride or lanthanum carboxylate for orthophosphate removal in seawater aquarium – a feasibility study
Einzelnachweise
- ↑ a b c d Datenblatt Lanthanchlorid bei Acros, abgerufen am 20. Juli 2010.
- ↑ a b c Jean DAns, Ellen Lax: Taschenbuch für Chemiker und Physiker, Vols. 1–3: Elemente, anorganische Verbindungen und Materialien, Minerale, Vol. III, ISBN 978-3-540-60035-0, S. 1463 (Eingeschränkte Vorschau in der Google Buchsuche); abgerufen am 20. Juli 2010.
- ↑ Datenblatt Lanthanum(III) chloride bei Sigma-Aldrich, abgerufen am 20. Juli 2010.
- ↑ Lanthanum chloride (American Elements)
- ↑ a b Datenblatt Lanthanum(III) chloride bei Sigma-Aldrich, abgerufen am 7. April 2011.
- ↑ a b Datenblatt Lanthanum(III) chloride heptahydrat bei Sigma-Aldrich, abgerufen am 20. Juli 2010.
- ↑ Lanthanchlorid (Espi-Metal)
- ↑ Lanthanum chloride solution (Blue Line)
Kategorien:- Reizender Stoff
- Lanthanverbindung
- Chlorid
Wikimedia Foundation.

