- Rhenium(VII)-fluorid
-
Strukturformel 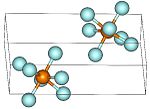
Allgemeines Name Rhenium(VII)-fluorid Andere Namen Rheniumheptafluorid
Summenformel ReF7 CAS-Nummer 17029-21-9 PubChem 123369 Kurzbeschreibung gelber Feststoff[1]
Eigenschaften Molare Masse 319,20 g·mol−1 Aggregatzustand fest
Dichte 4,3 g·cm−3[1]
Schmelzpunkt Siedepunkt 73,7 °C[1]
Sicherheitshinweise EU-Gefahrstoffkennzeichnung [2] keine Einstufung verfügbar R- und S-Sätze R: siehe oben S: siehe oben Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Rhenium(VII)-fluorid, meist auch Rheniumheptafluorid genannt, ist eine chemische Verbindung der Elemente Rhenium und Fluor und gehört zur Stoffgruppe der Fluoride. Es ist das einzige bekannte thermisch stabile Metall-Heptafluorid.[3]
Gewinnung und Darstellung
Rhenium(VII)-fluorid wird durch Reaktion aus den Elementen bei 400 °C dargestellt.[4]
Eigenschaften
Rhenium(VII)-fluorid ist ein bei niedrigen Temperaturen schmelzender gelber Feststoff. Er besitzt eine verzerrte pentagonal-bipyramidale Struktur ähnlich der von Iodheptafluorid.[5]
Einzelnachweise
- ↑ a b c d WebElements: Rheniumheptafluoride
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Greenwood, Norman N.; Earnshaw, Alan. (1997), Chemistry of the Elements (2nd ed.), Oxford: Butterworth-Heinemann, ISBN 0080379419
- ↑ A. F. Holleman; Wiberg, Egon; Wiberg, Nils: Inorganic Chemistry. Boston: Academic Press 2001, ISBN 0-12-352651-5
- ↑ Vogt T., Fitch A. N., Cockcroft J. K.: Crystal and Molecular Structures of Rhenium Heptafluoride. In: Science. 263, Nr. 5151, 1994, S. 1265. doi:10.1126/science.263.5151.1265. PMID 17817431.
RheniumhalogenideRhenium(III)-Verbindungen: Rhenium(III)-chlorid | Rhenium(III)-bromid | Rhenium(III)-iodid
Rhenium(IV)-Verbindungen: Rhenium(IV)-fluorid | Rhenium(IV)-chlorid | Rhenium(IV)-bromid | Rhenium(IV)-iodid
Rhenium(V)-Verbindungen: Rhenium(V)-fluorid | Rhenium(V)-chlorid | Rhenium(V)-bromid
Rhenium(VI)-Verbindungen: Rhenium(VI)-fluorid | Rhenium(VI)-chlorid
Andere Oxidationsstufen: Rhenium(VII)-fluorid
Wikimedia Foundation.
Schlagen Sie auch in anderen Wörterbüchern nach:
Rhenium(VI)-fluorid — Strukturformel Allgemeines Name Rhenium(VI) fluorid Andere Namen … Deutsch Wikipedia
Rhenium — Eigenschaften … Deutsch Wikipedia
Chemikalienliste — Die Chemikalienliste stellt eine alphabetisch sortierte Liste von Chemikalien dar, ohne Anspruch auf Vollständigkeit. Elemente sind fett gekennzeichnet, Stoffgruppen kursiv. Der Haupteintrag zu einer Chemikalie ist gleichzeitig der Name des… … Deutsch Wikipedia
Liste chemischer Verbindungen — Die Chemikalienliste stellt eine alphabetisch sortierte Liste von Chemikalien dar, ohne Anspruch auf Vollständigkeit. Elemente sind fett gekennzeichnet, Stoffgruppen kursiv. Der Haupteintrag zu einer Chemikalie ist gleichzeitig der Name des… … Deutsch Wikipedia
Liste von chemischen Verbindungen — Die Chemikalienliste stellt eine alphabetisch sortierte Liste von Chemikalien dar, ohne Anspruch auf Vollständigkeit. Elemente sind fett gekennzeichnet, Stoffgruppen kursiv. Der Haupteintrag zu einer Chemikalie ist gleichzeitig der Name des… … Deutsch Wikipedia
Liste der anorganischen Verbindungen — Liste der Namen von anorganischen Verbindungen, für die es einen Wikipedia Artikel gibt. Die Trivialnamen anorganischer Verbindungen sind jedoch nur dann in dieser Liste aufgeführt, wenn lediglich dieser Name und nicht der offizielle chemische… … Deutsch Wikipedia
Osmium — Eigenschaften … Deutsch Wikipedia
Kalifornium — Eigenschaften … Deutsch Wikipedia
Bindefähigkeit — Die Wertigkeit oder Valenz eines Atoms oder einer Gruppe von Atomen innerhalb einer chemischen Verbindung wurde 1852 vom englischen Chemiker Edward Frankland eingeführt und gab ursprünglich an, wie viele Atome Wasserstoff das Atom oder die Gruppe … Deutsch Wikipedia
Einwertig — Die Wertigkeit oder Valenz eines Atoms oder einer Gruppe von Atomen innerhalb einer chemischen Verbindung wurde 1852 vom englischen Chemiker Edward Frankland eingeführt und gab ursprünglich an, wie viele Atome Wasserstoff das Atom oder die Gruppe … Deutsch Wikipedia

