- Triptycen
-
Strukturformel 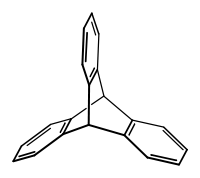
Allgemeines Name Triptycen Andere Namen - 9,10-Dihydro-9,10[1’,2’]-benzenoanthracen
- Tribenzobicyclo[2.2.2]octatrien
- NSC122926
- 9,10-dihydro-477-75-8
- 9,10[1’,2’]-Benzenoanthracen
Summenformel C20H14 CAS-Nummer 477-75-8 PubChem 92764 Kurzbeschreibung Farblose Kristalle[1]
Eigenschaften Molare Masse 254,33 g·mol−1 Schmelzpunkt Sicherheitshinweise EU-Gefahrstoffkennzeichnung [2] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: keine S-Sätze Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Triptycen gehört zur Klasse der aromatischen Kohlenwasserstoffe, deren Grundgerüst aus den Barrelenen besteht. Es ist das formale Produkt einer Diels-Alder-Reaktion von Anthracen mit Didehydrobenzen, einem Arin. Die Verbindung besitzt eine Schaufelrad-Konfiguration mit D3h-Symmetrie. Das Kohlenwasserstoffgerüst ist äußerst rigide, so dass Triptycen und Triptycen-Derivate, wie beispielsweise Triptycenchinon,[3] in organischen Verbindungen als molekulares Gerüst in der Synthese bestimmter molekularer Motoren eingesetzt[4] oder als spezielle Ligandensysteme für zum Beispiel Hydrocyanierungsreaktionen[5][6] eingesetzt werden können.
Geschichte
Paul D. Bartlett und Mitarbeiter publizierten die Synthese 1942 und benannten sie nach „The triptych of antiquity“, übersetzt „Das Triptychon der Antike“, einem Buch bestehend aus drei an einer Achse zusammen befestigten Seiten.
Gewinnung und Darstellung
Die ursprüngliche Synthese des Triptycens verlief über sieben Stufen, beginnend mit Anthracen und p-Benzochinon.
Einzelnachweise
- ↑ a b Thieme Chemistry (Hrsg.): RÖMPP Online - Version 3.5. Georg Thieme Verlag KG, Stuttgart 2009.
- ↑ Datenblatt Triptycen bei Sigma-Aldrich, abgerufen am 1. September 2009.
- ↑ Triptycene quinones in synthesis: preparation of triptycene bis-cyclopentenedione Spyros Spyroudis and Nikoletta Xanthopoulou Arkivoc 2003 (vi) 95–105 Online article
- ↑ Kelly TR, De Silva H, Silva RA: Unidirectional rotary motion in a molecular system. In: Nature. 401, Nr. 6749, September 1999, S. 150–152. doi:10.1038/43639. PMID 10490021. Abgerufen am 16. Juli 2008.
- ↑ Bini L, Müller C, Wilting J, von Chrzanowski L, Spek AL, Vogt D: Highly selective hydrocyanation of butadiene toward 3-pentenenitrile. In: J. Am. Chem. Soc.. 129, Nr. 42, Oktober 2007, S. 12622–12623. doi:10.1021/ja074922e. PMID 17902667. Abgerufen am 16. Juli 2008.
- ↑ In dieser Reaktion ist das Substrat 1,3-Butadien, der Reaktionspartner Acetoncyanhydrin, der Katalysator Ni(cod)2 und der Ligand ein zweizähniges Organophosphin mit einem großen Griffwinkel auf einem Triptycengerüst.
Wikimedia Foundation.
