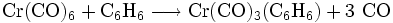- Chromcarbonyl
-
Strukturformel 
Allgemeines Name Chromhexacarbonyl Andere Namen Chromcarbonyl
Summenformel C6CrO6 CAS-Nummer 13007-92-6 PubChem 518677 Kurzbeschreibung weißer Feststoff[1] Eigenschaften Molare Masse 220,06 g·mol−1 Aggregatzustand fest
Dichte 1,77 g/cm3 (20 °C)[1]
Schmelzpunkt Siedepunkt 210 °C (Zersetzung)[1]
Dampfdruck Löslichkeit sehr schlecht in Wasser[1]
Sicherheitshinweise Gefahrstoffkennzeichnung [1] 
Giftig (T) R- und S-Sätze R: 45-5-22 S: 53-45-36 MAK nicht vergeben, da Verdacht auf kregserzeugende Wirkung[1]
LD50 150 mg/kg (Maus, oral)[1]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Chromhexacarbonyl ist eine komplexe chemische Verbindung. Sie besteht aus einem zentralen Chromatom in der Oxidationsstufe null, um welches sechs Carbonylliganden koordiniert sind.
Inhaltsverzeichnis
Eigenschaften
Das Chromatom ist im Komplex oktaedrisch von sechs Carbonylliganden umgeben. Der Cr-C-Abstand beträgt 192 pm.[2] Es handelt sich um einen stabilen 18-Valenzelektronenkomplex, der bei 150 °C unzersetzt schmilzt. Chromhexacarbonyl ist eine toxische Verbindung die sich bei schnellem Erhitzen und Temperaturen über 210 °C explosiv zersetzen kann. Des Weiteren besteht der Verdacht auf eine cancerogene Wirkung.[1]
Die Carbonylliganden können oxidativ, photolytisch oder thermisch abgespalten werden. Die entstehenden freien Koordinationsstellen können durch Lösungsmittelmoleküle besetzt werden. So entsteht beim Erhitzen in aromatischen Lösungsmitteln durch Abspaltung von drei Carbonylliganden ein neuer Komplex der einen aromatischen Liganden besitzt.
Die Bildung solcher Komplexe ist für elektronenreiche Aromaten begünstigt.
Auch andere Lösungsmitteln, die zu einer Koordination befähigt sind, können als labile Liganden am Komplex koordinieren.
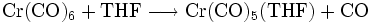
- Abspaltung eines Carbonylliganden beim Erhitzen in Tetrahydrofuran
Verwendung
Chromhexacarbonyl kann zur Herstellung chromhaltiger Fischer-Carbene benutzt werden. Hierzu wird es mit Kohlenstoff-Nukleophil, wie beispielsweise Lithiumalkylen umgesetzt, die sich an den Carbonylkohlenstoff addieren. Eine wichtige Anwendung ist die Dötz-Reaktion, die in der Synthese von aromatischen Verbindungen, wie Vitamin K oder Vitamin E eine Bedeutung hat.
Literatur
- Christoph Elschenbroich: Organometallchemie. 5. Auflage, Teubner Wiesbaden 2005, ISBN 3-519-53501-7.
Quellen
Wikimedia Foundation.