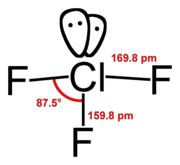
- ClF3
-
Strukturformel 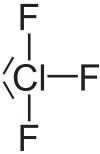
Allgemeines Name Chlortrifluorid Andere Namen Chlor(III)-fluorid
Summenformel ClF3 CAS-Nummer 7790-91-2 PubChem 24637 Kurzbeschreibung farbloses stechend riechendes Gas Eigenschaften Molare Masse 92,45 g·mol−1 Aggregatzustand gasförmig
Dichte 3,57 kg·m–3 (Gasdichte bei 0 °C)[1]
Schmelzpunkt -76,31 °C[1]
Siedepunkt 11,8 °C[1]
Dampfdruck 1,419 Bar (20 °C)[1]
Sicherheitshinweise Gefahrstoffkennzeichnung [1] 


Brand-
förderndGiftig Ätzend (O) (T) (C) R- und S-Sätze R: 9-23-35 S: 17-26-36-45 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Chlortrifluorid ist eine Interhalogenverbindung. Es handelt sich um ein farbloses, giftiges, stechend riechendes, ätzendes Gas, das in feuchter Luft weiße Nebel entwickelt. Es ist wie alle Interhalogenverbindungen sehr reaktionsfreudig.
Inhaltsverzeichnis
Eigenschaften
Chlortrifluorid ist ein farbloses Gas, das bei ca. 12 °C in den flüssigen Zustand übergeht und bei -76,3 °C erstarrt. Mit Wasser reagiert Chlortrifluorid unter Sauerstofffreisetzung. Chemisch verhält sich Chlortrifluorid wie ein starkes Oxidationsmittel, es greift Metalle unter Fluoridbildung an. Die weitere Reaktion mit Metallen hängt davon ab, ob die gebildete Fluoridschicht stabil ist; bei Kupfer ist dies der Fall, sodass die Herstellung in Kupfergefäßen erfolgt. Nichtmetalle bilden keine Schutzschicht, sondern werden in Brand gesetzt.
Chlortrifluorid greift auch die Füllstoffe der Atemschutzfilter (Aktivkohle) an.
Verwendung
Chlortrifluorid kann zur Fluorierung und als Oxidator für einige Raketentreibstoffe (High-energy-fuel) verwendet werden. [2] Darüber hinaus wird es, zur Erhöhung der Verbrennungstemperatur, Schweißgasen zugesetzt und wurde im zweiten Weltkrieg unter der Deckbezeichnung „N-Stoff“ in Deutschland produziert, wobei die Verwendung als Kampfstoff oder als brandstiftendes Mittel in Erwägung gezogen wurde.
Toxikologie
Als Inhalationsgift wirkt es auf den gesamten Atemtrakt. Die Folgen sind Aufblähungen und Schwellungen der Lunge, Verätzungen der oberen Atemwege bis hin zur eitrigen Bronchitis. Hohe Konzentrationen führen zu starkem Reizhusten und schwersten Lungenschädigungen. Gasförmiges Chlor(III)-fluorid greift die Augen sehr stark an; die Schädigungen führen zur Hornhauttrübung.
Siehe auch
Referenzen
- ↑ a b c d e Eintrag zu Chlortrifluorid in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 4.1.2008 (JavaScript erforderlich)
- ↑ Eintrag über die Chlorfluoride in der Onlineversion des Römpp Chemielexikons (kostenpflichtige Registrierung erforderlich)
Wikimedia Foundation.