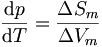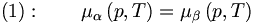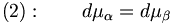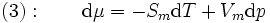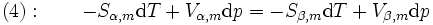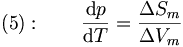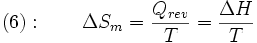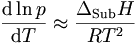- Clapeyronsche Gleichung
-
Mit der Clapeyron-Gleichung, die Benoit Clapeyron 1834 entwickelte, erhält man die Steigung von Phasengrenzlinien in einem Phasendiagramm. Sie lässt sich für verschiedene Fälle spezifizieren. Aus der Clapeyron-Gleichung wurde auch die Clausius-Clapeyron-Gleichung entwickelt. Die Clapeyron-Gleichung lautet:
Herleitung
An einer Phasengrenzlinie, d.h. bei dem Wertepaar aus Temperatur T und Druck p, in dem zwei Phasen α und β im Gleichgewicht koexistieren, besitzen diese beiden Phasen die gleichen chemischen Potentiale, es gilt:
Um nun die Steigung der Phasengrenzlinien bestimmen zu können, gilt es die Funktion dp / dT zu finden, die diese beschreibt. Da auf der gesamten Phasengrenzlinie gilt, dass auch bei infinitesimalen Veränderung von p oder T die Gleichung 1 gilt, muss auch die Veränderung der Potentiale μα und μβ immer gleich bleiben. Mathematisch bedeutet das:
Aus der Gibbs-Duhem-Gleichung ist bekannt, dass
wobei Sm und Vm die molare Entropie bzw. das molare Volumen sind. Setzt man nun dies in Gleichung 2 ein, so erhält man
Durch Ausklammern von dp und dT sowie anschließender Umformung erhält man nun die Clapeyron-Gleichung:
Wobei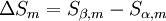 bzw.
bzw. 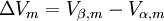 sind. Im Unterschied zur Clausius-Clapeyron-Gleichung gilt die Clapeyron-Gleichung für jedes Phasengleichgewicht, d.h. auch z.B. zwischen zwei festen Phasen, eines reinen Stoffes.
sind. Im Unterschied zur Clausius-Clapeyron-Gleichung gilt die Clapeyron-Gleichung für jedes Phasengleichgewicht, d.h. auch z.B. zwischen zwei festen Phasen, eines reinen Stoffes.Für reversible Vorgänge kann die Umwandlungsentropie aus der dabei umgesetzten Wärmemenge Qrev berechnet werden, die bei isobaren Vorgängen gleich der Änderung der molaren Enthalpie
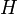 ist:
ist:Damit erhält man aus der Clapeyron-Gleichung die Clausius-Clapeyron-Gleichung.
Die Clapeyron-Gleichung gilt für alle Phasenübergänge. Insbesondere werden die folgenden Phasengrenzlinien durch sie bestimmt:- fest/flüssig, siehe Schmelzpunkt.
- flüssig/gasförmig, siehe auch Clausius-Clapeyron-Gleichung, unter Verwendung der Verdampfungsenthalpie.
- fest/gasförmig, unter Verwendung der Sublimationsenthalpie. Man erhält folgende Beziehung für die Temperaturabhängigkeit des Sublimationsdampfdrucks:
Wikimedia Foundation.