- 1,1,1-Trifluorethan
-
Strukturformel 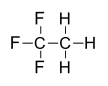
Allgemeines Name 1,1,1-Trifluorethan Andere Namen - R 143a
- Freon 143a
Summenformel C2H3F3 CAS-Nummer 420-46-2 PubChem 9868 Kurzbeschreibung farbloses Gas mit süßlichem Geruch[1]
Eigenschaften Molare Masse 84,04 g·mol−1 Aggregatzustand gasförmig
Dichte 3,822 kg·m−3 (0 °C) [1]
Schmelzpunkt −111,3 °C [1]
Siedepunkt −47,2 °C [1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [2] 

Gefahr
H- und P-Sätze H: 280-220 EUH: keine EUH-Sätze P: ? EU-Gefahrstoffkennzeichnung [1] 
Hoch-
entzündlich(F+) R- und S-Sätze R: 12 S: 9-16-33 GWP 4470 (bezogen auf 100 Jahre)[3]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Trifluorethan ist eine gasförmige organisch-chemische Verbindung aus der Gruppe der Fluorkohlenwasserstoffe (FKW).
Inhaltsverzeichnis
Eigenschaften
Trifluorethan ist ein hochentzündliches Gas, welches mit Luft explosionsfähige Gemische bildet. Der Explosionsbereich liegt zwischen 9,5 Vol% als untere Explosionsgrenze (UEG) und 19 Vol% als obere Explosionsgrenze (OEG).[4] Mit einer relativen Gasdichte von 2,96 (Luft = 1)[4] ist das Gas schwerer als Luft und sammelt sich deshalb am Boden.[1] Die Dampfdrücke bei verschiedenen Temperaturen sind in folgender Tabelle angegeben:[1]
T in °C −10 10 20 30 50 70 p in bar 4,4 8,3 11,1 14,4 23,1 35,3 Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 4,02423, B = 786,645 und C = −30,093 im Temperaturbereich von 174 K bis 226 K.[5]
Zusammenstellung der wichtigsten thermodynamischen Eigenschaften Eigenschaft Typ Wert [Einheit] Bemerkungen Standardbildungsenthalpie ΔfH0gas −748,7 kJ·mol−1[6] Verbrennungsenthalpie ΔcH0gas −1008 kJ·mol−1[7] Wärmekapazität cp 109,66 J·mol−1·K−1 (220 K)[8] als Flüssigkeit Tripelpunkt Ttriple 161,82 K [8] Kritische Temperatur Tc 345,86 K [9] Kritischer Druck pc 37,64 bar [9] Kritische Dichte ρc 5,16 mol·l−1[9] Verwendung
C2H3F3 findet als Kältemittel Verwendung.
Umwelt
Difluormethan ist als Treibhausgas 4470-mal stärker als CO2. Im Gegensatz zu den Fluorchlorkohlenwasserstoffen ist es aber nicht ozonschädigend. Im Kyoto-Protokoll ist es als „wasserstoffhaltiger Fluorkohlenwasserstoff“ benannt, dessen Emission reduziert werden muss.
Einzelnachweise
- ↑ a b c d e f g Eintrag zu Trifluorethan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3. März 2008 (JavaScript erforderlich).
- ↑ Gerling Holz & Co: Sicherheitsdatenblatt
- ↑ P. Forster, V. Ramaswamy et al.: Changes in Atmospheric Constituents and in Radiative Forcing. In: Climate Change 2007: The Physical Science Basis. Contribution of Working Group I to the Fourth Assessment Report of the Intergovernmental Panel on Climate Change. Cambridge University Press, Cambridge und New York 2007, S. 212; (PDF).
- ↑ a b G. Sorbe: Sicherheitstechnische Kenndaten chemischer Stoffe. - 82. Ergänzungslieferung 6/2001, ecomed Verlag Heidelberg, ISBN 3-609-73060-9.
- ↑ H. Russell Jr., D. R. V. Golding, D. M. Yost: The heat capacity, heats of transition, fusion and vaporization, vapor pressure and entropy of 1,1,1-trifluoroethane. In: J. Am. Chem. Soc. 66 (1944) S. 16-20. doi:10.1021/ja01229a006.
- ↑ E. Wu, A. S. Rodgers: Thermochemistry of gas-phase equilibrium CF3CH3 + I2 = CF3CH2I + HI. The carbon-hydrogen bond dissociation energy in 1,1,1-trifluoroethane and the heat of formation of the 2,2,2-trifluoroethyl radical. in J. Phys. Chem., 1974, 78, S. 2315-2317.
- ↑ V. P. Kolesov, A. M. Martynov, S. M. Skuratov: Standard enthalpy of formation of 1,1,1-trifluoroethane. In: Russ. J. Phys. Chem. (Engl. Transl.) 39 (1965) 39, S. 223-225.
- ↑ a b H. Russell Jr., D. R. V. Golding, D. M. Yost: The heat capacity, heats of transition, fusion and vaporization, vapor pressure and entropy of 1,1,1-trifluoroethane. In: J. Am. Chem. Soc. 1944, 66, S. 16-20.
- ↑ a b c K. Fujiwara, S. Nakamura, M. Noguchi: Critical Parameters and Vapor Pressure Measurements for 1,1,1-Trifluoroethane (R-143a). In J. Chem. Eng. Data 43 (1998) S. 55-59, doi:10.1021/je970177h.
Kategorien:- Feuergefährlicher Stoff
- Fluoralkan
- Kühlmittel
Wikimedia Foundation.
