- Phenolrot
-
Strukturformel 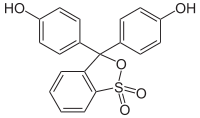
Allgemeines Name Phenolrot Andere Namen - Phenolsulfonphthalein
- 4,4-(3H-2,1-Benzoxathiol-3- yliden)bisphenol-1,1-dioxid)
Summenformel C19H14O5S CAS-Nummer 143-74-8 PubChem 4766 Kurzbeschreibung roter Feststoff mit schwachem Geruch[1]
Eigenschaften Molare Masse 354,38 g·mol−1 Aggregatzustand fest
Schmelzpunkt Löslichkeit sehr schlecht in Wasser (0,77 g·l−1 bei 100 °C)[1]
Sicherheitshinweise EU-Gefahrstoffkennzeichnung [1] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: keine S-Sätze Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Phenolrot ist ein Triphenylmethanfarbstoff und bildet die Basisverbindung der Familie der Sulfonphthaleine. Es wird als pH-Indikator eingesetzt und besitzt zwei Umschlagsbereiche. Bei pH ≈ 0,9 ändert sich die Farbe von rot auf gelb und bei pH ≈ 6,4–8,2 dann von gelb auf rotviolett.[2][3]
Inhaltsverzeichnis
Darstellung
In einer Friedel-Crafts-Acylierung werden 2 Äquivalente Phenol und 1 Äquivalent o-Sulfobenzoesäureanhydrid in Gegenwart geringer Mengen konzentrierter Schwefelsäure oder Zinkchlorid umgesetzt.
Eigenschaften
Phenolrot enthält zwei Hydroxylgruppen und einen wenig stabilen Sultonring. Im wässrigen Medium wird dieser Ring gespalten, und nach einer Umlagerung entsteht die chinoide gelb gefärbte Form des Farbstoffs. Dieses chinoide System kann im stark sauren Milieu (pH < 1) protoniert werden, wodurch die Lösung sich rot färbt. Im neutralem Milieu (pH = 6,4–8,3) wird die Hydroxygruppe deprotoniert und die Lösung färbt sich rotviolett.[2][4] Im stark basischen Bereich (pH > 14) erfolgt eine Anlagerung einer OH-Gruppe unter Bildung einer Triphenylmethanolstruktur. Phenolrot liegt dann als farbloses Trianion vor. [5]
Die Strukturen des Phenolrots Spezies H2In HIn− In2− Struktur 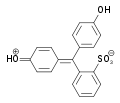
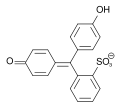
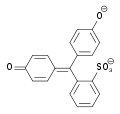
pH < 1 1–7,3 > 7,3 Farbe rot gelb rotviolett Verwendung
Phenolrot wird bei Säure-Base-Titrationen als Indikator eingesetzt, mit einem Umschlagsbereich zwischen pH 6,4 und 8,2. Der Farbwechsel erfolgt von rotviolett im Basischen nach gelb im Sauren.
Phenolrot dient als pH-Indikator für Zellkulturmedien.
Einzelnachweise
- ↑ a b c d Datenblatt Phenolrot bei Merck, abgerufen am 17. April 2010.
- ↑ a b Udo R. Kunze: Grundlagen der quantitativen Analyse, 3. Auflage, Georg Thieme Verlag, Stuttgart 1990, S. 96.
- ↑ Sulfonphtaleine – Phenolrot (Markus Weinmann, Max Planck Institut)
- ↑ K. Yamaguchi, Z. Tamura, M. Maeda: Molecular Structure of the Zwitterionic Form of Phenolsulfonphthalein, in: Analytical Sciences, 1997, 13 (3), S. 521–522.
- ↑ http://www.bdsoft.de/demo/index.htm?/demo/chemie/chemikalien/p/phenolrot.htm
Literatur
- Z. Tamura, M. Maeda: Differences between phthaleins and sulfonphthaleins, in: Yakugaku Zasshi, 1997, 117 (10–11), S. 764–770. (jap.); PMID 9414589
Weblinks
Wikimedia Foundation.
