- Rasch progressive Glomerulonephritis
-
Bei der rasch progressiven Glomerulonephritis (engl. rapidly progressive glomerulonephritis, kurz RPGN) handelt es sich um eine schubweise auftretende extrakapilläre Glomerulonephritis, die mit einem raschen Verlust der Nierenfunktion einhergeht. Unbehandelt kann es innerhalb von Wochen bis Monaten zum Nierenversagen kommen. Weitere Synonyme für diese Erkrankung sind rasch progrediente Glomerulonephritis und crescentic glomerulonephritis (engl. bogenförmige Glomerulonephritis).
Inhaltsverzeichnis
Epidemiologie
Inzidenz: < 1/100.000 / Jahr
Pathologie
Pathogenese
Es handelt sich bei der RPGN um ein Immunkomplexglomerulonephritis oder eine Antibasalmembran-Glomeruolonephritis. Die RPGN kann ohne erkennbaren Grund (idiopathisch) oder häufiger bei Systemerkrankungen wie der Wegener-Granulomatose, Goodpasture-Syndrom oder der Panarteriitis nodosa auftreten.
Makroskopisch
Die Nieren sind eventuell leicht vergrößert und weisen einzelne punktförmigen Blutungen auf.
Mikroskopisch
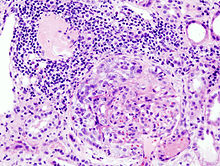
Das histologische Bild, das sich zeigt, ist bunt, da die Erkrankung schubweise verläuft. Typisch ist die ausgeprägte Halbmondbildung in den Glomeruli. Weiterhin sind einzelne Monozyten zu finden. Die Umgebung des Glomerulus ist meist entzündlich infiltriert. In der elektronenmikroskopischen Aufnahme zeigen die Gomerulusschlingen sich rupturiert und der Kapselraum des Glomerulus ist mit Fibrin ausgefüllt. Mit einer bestimmten Färbemethode, der Immunfluoreszenz lassen sich die Anlagemuster der Immnunglobuline nachweisen, dies wird benutzt, um die verschiedenen Formen der RPGN zu unterscheiden (s. u.).
Die ANCA-assoziierte rasch progressive Glomerulonephritis wird nach dem Anteil der Glomeruli mit entzündlichen Halbmonden und dem Anteil vernarbter Glomeruli (globale Sklerose) eingeteilt in:
Klasse Einschlusskriterien Fokal ≥ 50% normale Glomeruli Halbmondbildung ≥ 50% Glomeruli mit zellulären Halbmonden Gemischt < 50% normale, < 50% sklerotische < 50% Glomeruli mit Halbmonden Sklerotisch ≥ 50% komplett vernarbte Glomeruli Diese Einteilung erlaubt eine Abschätzung der Prognose: Patienten mit fokaler ANCA-assoziierter Glomerulonephritis haben die beste Prognose. Patienten mit vorwiegender Halbmondbildung haben ein hochakutes frühes Krankheitsstadium, die Chance, dass die Erkrankung auf eine immunusuppressive Therapie anspricht, sind aber relativ gut. Die Prognose der Mischform ist schlechter. Patenten mit einem hohen Anteil vernarbter Glomeruli befinden sich bereits in einem fortgeschrittenen Krankheitsstadium, die Chance, dass dieses auf eine Behandlung anspricht, sind gering.[1]
Einteilung
Es wird zwischen drei Formen der RPGN unterschieden:
- Antibasalmembran GN (10–20%), Nachweis von Antikörpern gegen die Basalmembran im Serum, histologischer Nachweis von Immunglobulinen Typ G und C3-Komplement in linearer Anordnung an der Basalmembran.
-
- ohne Lungenbeteiligung, sehr selten
- mit Lungenbeteiligung = Goodpasture-Syndrom, oft Männer vor dem 40. Lebensjahr
-
- Immunkomplex (30–40%), Anlagerung von Immunkomplexen in Haufen (sogenannte "Humps"), z. B. bei Lupus erythematodes
- ANCA-assoziierte Vaskulitis (40–50%), z. B. als renale Verlaufsform der Wegener-Granulomatose
Klinik
- Rascher Beginn, Hypertonie,
- Nierenversagen bis zu Dialysepflichtigkeit innerhalb von Wochen bei sonographisch nicht vergrößerten Nieren,
- Proteinurie mit eventuellem nephrotischem Syndrom,
- Lungenblutungen bei Goodpasture-Syndrom
Diagnose
Die Klinik und rasch ansteigende Retentionswerte, immunologische Diagnostik (s. o.). Nierenbiopsie mit folgender Histologie kann die Diagnose sichern. Die Differentialdiagnosen sind das akute Nierenversagen (Anamnese des auslösenden Ereignisses) und die akute abakterielle Nephritis, hier sollte dann die Medikamenteneinnahme erfragt werden.
Durch die exakte Bestimmung antizytoplasmatischer Antikörper gegen neutrophile Granulozyten (ANCA) und entsprechenden Verteilungsmustern lässt sich die Ursache der RPGN differenzieren. Bei sich der der Wegener-Granulomatose finden sich c-ANCA. Bei dem Typ p-ANCA sollte eher an eine mikroskopische Polyangiitis gedacht werden.
Therapie
Entsprechend der Immunpathogenese besteht die Therapie aus einer hoch dosierten Immunsuppression mit Steroiden in Kombination mit Cyclophosphamid. Das Goodpasture-Syndrom wird in Kombination mit Plasmaseparation behandelt.
Die auftretende Niereninsuffizienz muss mit der Dialyse behandelt werden.
Verlauf und Prognose
Der Verlauf und die Prognose hängt vom Therapiebeginn ab. Das Vorliegen der dialysepflichtige Niereninsuffizienz oder bei einer Fibrose des Interstitiums sind prognostisch ungünstig.
Beim Goodpasture-Syndrom (Antikörper gegen die Basalmembranen von Lungenalveolen und Glomeruli) können pulmonale und renale Symptomatik zusammen, aber auch getrennt vorkommen. Es kommt zu Lungeninfiltraten, Bluthusten, mikrozytärer Anämie und zu einem progredienten Nierenversagen.
Das Goodpasture-Syndrom führt unbehandelt innerhalb weniger Tage zum Tode. Bei frühzeitiger Diagnose und Therapie hat sich die Prognose deutlich gebessert.
Komplikationen
Entwicklung einer terminalen Niereninsuffizienz mit Lungenödem, Hypertonie, Hyperkaliämie, evtl. Lungenblutungen.
Quellen
Einzelnachweise
- ↑ Annelies E Berden, et al.: Histopathologic classification of ANCA-associated glomerulonephritis. In: Journal of the American Society of Nephrology: JASN. 21, Nr. 10, 2010-10, S. 1628-1636. doi:10.1681/ASN.2010050477. Abgerufen am 11. Dezember 2010.
Literatur
- Riede, Schäfer: Pathologie. ISBN 3-1368-3303-1
- Herold: Innere Medizin. 2009 (Epidemiologie)
Weblinks
- Rasch progressive Glomerulonephritis Pathologie – Bilddatenbank Pathopic der Universität Basel – PathoPic-Anleitung (PDF)

Bitte den Hinweis zu Gesundheitsthemen beachten! Kategorie:- Krankheitsbild in der Nephrologie
- Antibasalmembran GN (10–20%), Nachweis von Antikörpern gegen die Basalmembran im Serum, histologischer Nachweis von Immunglobulinen Typ G und C3-Komplement in linearer Anordnung an der Basalmembran.
Wikimedia Foundation.