- Silber(I)-fluorid
-
Kristallstruktur 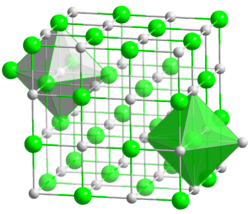
__ Ag+ __ F− Allgemeines Name Silber(I)-fluorid Andere Namen - Silberfluorid
- Silbermonofluorid
Verhältnisformel AgF CAS-Nummer 7775-41-9 Kurzbeschreibung gelber Feststoff[1]
Eigenschaften Molare Masse 126,87 g·mol−1 Aggregatzustand fest
Dichte Schmelzpunkt Siedepunkt 1150 °C[2]
Löslichkeit sehr gut in Wasser (etwa 1850 g·l−1 bei 15,5 °C)[2]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [3] 

Gefahr
H- und P-Sätze H: 301-311-315-318-331 EUH: keine EUH-Sätze P: 261-280-301+310-305+351+338-311 [3] EU-Gefahrstoffkennzeichnung [2] 

Giftig Ätzend (T) (C) R- und S-Sätze R: 23/24/25-34 S: 26-28-36/37/39-45 MAK 0,01 mg·m−3[2]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Silber(I)-fluorid ist das Silbersalz der Fluorwasserstoffsäure. Im Gegensatz zu den anderen Halogeniden des Silbers ist es weniger lichtempfindlich, sehr gut in Wasser löslich und hygroskopisch.
Inhaltsverzeichnis
Gewinnung und Darstellung
Das Silber(I)-fluorid kann sowohl aus den Elementen Silber und Fluor als auch aus Silber(I/III)-oxid (AgO), Silber(I)-oxid (Ag2O) und Silber(I)-carbonat (Ag2CO3) jeweils mit Fluorwasserstoff erhalten werden:[4]

- Silber(I)-oxid reagiert mit Fluorwasserstoff zu Silber(I)-fluorid und Wasser.
Eigenschaften
Wie Silberchlorid und Silberbromid kristallisiert AgF in der kubischen NaCl-Struktur. Im Gegensatz zu den anderen Silberhalogeniden kann AgF aus wässrigen Lösungen als verschiedene Hydrate kristallisieren (AgF · H2O, AgF · 2 H2O und AgF · 4 H2O). Mit überschüssiger Fluorwasserstoffsäure bilden sich AgF · HF und AgF · 3 HF. In einem Liter Wasser lösen sich bei Raumtemperatur (25 °C) 1,8 kg AgF, wobei Silberf(I)-fluorid in Silber- und Fluoridionen dissoziiert:
Die Bildungsenthalpie aus den Elementen (∆Hf) beträgt −204 kJ.
Verwendung
Silber(I)-fluorid wird vor allem in der Fotografie angewendet, wobei Farbfilme mit dem besonders im UV-Bereich empfindlichen AgF beschichtet werden.[5] Silber(I)-fluorid dient als mildes Fluoridierungsmittel für Elementhalogenide und bei der Herstellung von Organofluorverbindungen durch Addition von Fluor an Doppelbindungen. Als Beispiel sei die Anlagerung von AgF an Perfluoroalkene in Acetonitril erwähnt, bei der Perfluoroalkylsilber(I)-Verbindungen entstehen: R–CF=CF2 + AgF → R–(CF–CF3)Ag.[6]
Auch bei der Behandlung von Karies wird AgF oder dessen Diamminkomplex unter dem Namen Saforide eingesetzt (siehe Weblinks).
Sicherheitshinweise
Die Handhabung von Silber(I)-fluorid ist nicht ungefährlich, da es beispielsweise mit Silicium, Titan und Calciumhydrid unter starker Hitzeentwicklung reagiert. Bei Kontakt mit Bor und Natrium besteht sogar Explosionsgefahr. Des Weiteren wirkt es ätzend auf Augen und Haut bzw. bei Einatmung in die Lunge.[2]
Siehe auch
Einzelnachweise
- ↑ Nils Wiberg, Egon Wiberg, Arnold Fr. Holleman: Lehrbuch der Anorganischen Chemie. 102 Auflage. de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1344.
- ↑ a b c d e f g Eintrag zu CAS-Nr. 7775-41-9 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 21.01.07 (JavaScript erforderlich)
- ↑ a b Datenblatt Silver(I) fluoride bei Sigma-Aldrich, abgerufen am 23. April 2011.
- ↑ G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry 2nd ed., vol. 1, Academic Press 1963, S. 240-1.
- ↑ N. N. Greenwood, A. Earnshaw. Chemie der Elemente. 1. korr. Auflage. VCH, Weinheim, 1990, S. 1516, ISBN 3-527-26169-9
- ↑ W. T. Miller, , Burnard, R. J. (1968) J. Am. Chem. Soc. 90, 7367–7368.
Weblinks
Kategorien:- Giftiger Stoff
- Ätzender Stoff
- Silberverbindung
- Fluorid
- Fotografie
Wikimedia Foundation.

