- Thalliumbromidiodid
-
Kristallstruktur 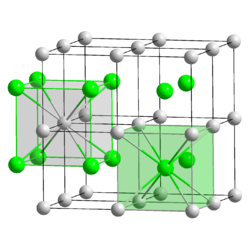
__ Tl+ __ Br− und I− Kristallsystem kubisch
Raumgruppe 
Koordinationszahlen Cs[8], Br und I[8]
Allgemeines Name Thalliumbromidiodid Andere Namen - KRS-5
- Thalliumbromoiodid
Verhältnisformel Tl(Br,I) CAS-Nummer - 7789-40-4 (TlBr)
- 7790-30-9 (TlI)
Kurzbeschreibung roter, geruchloser Feststoff[1]
Eigenschaften Molare Masse 311,53 g·mol−1
(Mittelwert bei 42% TlBr und 58% TlI)Aggregatzustand fest
Dichte 7,37 g·cm−3 [2]
Schmelzpunkt Löslichkeit - schlecht in Wasser (0,5 g·l−1 bei 20 °C)[2]
- löslich in Ethylenglycol und Dimethylsulfoxid[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [3][4] 


Gefahr
H- und P-Sätze H: 300-330-373-411 EUH: keine EUH-Sätze P: 260-264-273-284-301+310-310 [3] EU-Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [5] 

Sehr giftig Umwelt-
gefährlich(T+) (N) R- und S-Sätze R: 26/28-33-51/53 S: (1/2)-13-28-45-61 MAK 0,1 mg·m−3 [1]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Thalliumbromidiodid Tl(Br,I), auch bekannt unter der in der Industrie verwendeten Codebezeichnung KRS-5, ist eine anorganisch-chemische Mischkristallverbindung. Man kann es als Mischverbindung aus Thallium(I)-bromid und Thallium(I)-iodid auffassen. Besondere Bedeutung hat diese Verbindung aufgrund ihrer außergewöhnlichen optischen Eigenschaften in der Infrarotspektroskopie.
Inhaltsverzeichnis
Eigenschaften
Industriell verwendetes Thalliumbromidiodid setzt sich typischerweise formal aus 42 % Thallium(I)-bromid und 58 % Thallium(I)-iodid zusammen und besitzt demnach eine mittlere molare Masse von 311,53 g/mol. In der Kristallstruktur nimmt Thallium (Tl+) 100 % der Kationen-Plätze ein, während die Anionen-Positionen statistisch zu 42 % von Bromid (Br−) und zu 58 % Iodid (I−) besetzt sind, es handelt sich also um einen Mischkristall.
Das rote Salz kristallisiert im kubischen Kristallsystem in der Raumgruppe
 und ist isotyp zur Caesiumchloridstruktur. Die Kristalle sind sehr weich, sie weisen nach Knoop eine Härte von nur 40 K auf (Vergleich: Diamant hat 7000 K). Ähnlich wie Kaliumbromid ist es ein kaltfließendes Material und daher leicht verformbar.
und ist isotyp zur Caesiumchloridstruktur. Die Kristalle sind sehr weich, sie weisen nach Knoop eine Härte von nur 40 K auf (Vergleich: Diamant hat 7000 K). Ähnlich wie Kaliumbromid ist es ein kaltfließendes Material und daher leicht verformbar.Thalliumbromidiodid weist eine hohe Brechzahl auf, die je nach Wellenlänge zwischen 2,73 (bei 0,5 µm) und 2,15 (bei 50 µm) liegt. Daraus resultieren relativ geringe Verluste bei der Reflexion (vgl. fresnelsche Gleichungen), so liegt der maximale Transmissionsgrad eines 1 mm dicken KRS-5-Fensters im infraroten Bereich bei etwa 72 % (2 Reflexionen).[6] Vergleicht man dies mit anderen Materialien, wie ZnSe, KBr oder AMTIR, so fällt auf, dass Thalliumbromidiodid eine etwa gleichbleibend hohe Transmissionsgrad über einen großen Wellenlängenbereich (2–50 µm) besitzt. Zum Vergleich, Quarzglas weist zwar einen höheren Transmissionsgrad auf, jedoch nur in kleineren Wellenlängenbereichen (90 % bei 0,3–2 µm; 80 % bei 100–600 µm). Diamant hingegen zeigt einen großen Bereich mit hohem Transmissionsgrad (bis zu 65 %), allerdings ist Diamant wesentlich teurer und schwieriger zu verarbeiten.
In Wasser löst es sich nur zu etwa 0,05 %. Dagegen ist es in einigen polaren, organischen Lösungsmitteln löslich, wie etwa Ethylenglycol oder Dimethylsulfoxid (DMSO). Zudem kann es sich in alkalisch-wässrigem Medium sowie bei Vorhandensein von Komplexbildnern lösen.
Verwendung
Die gute Durchlässigkeit für infrarotes Licht macht Thalliumbromidiodid zu einem idealen Material zur Herstellung von Fenstern, Linsen und Filtern für optische Geräte, die im Infrarotbereich arbeiten, zum Beispiel Infrarotkameras oder Infrarotspektrometer. Die hohe Brechzahl ermöglicht eine weitere Anwendung im infrarotspekroskopischen Bereich, die ATR-Spektroskopie, bei der die abgeschwächte Totalreflexion zur Untersuchung von Oberflächeneigenschaften genutzt wird.
Gefahren
Thalliumbromidiodid ist als Thalliumverbindung als potentiell giftig anzusehen. Allein seine geringe Löslichkeit in Wasser, bedingt durch den Gehalt an Thallium(I)-iodid, macht seine Handhabung im Bereich der Spektroskopie sicherer. Besondere Vorsicht sollte jedoch geboten sein, denn Thalliumbromidiodid löst sich in einigen organischen Lösungsmitteln. Gelöste Thalliumsalze sind außerordentlich giftig.
Einzelnachweise
- ↑ a b c Sicherheitsdatenblatt (Korth)
- ↑ a b c Datenblatt von Korth Kristalle GmbH
- ↑ a b Datenblatt Thallium(I) bromide bei Sigma-Aldrich, abgerufen am 24. April 2011.
- ↑ Datenblatt Thallium(I) iodide bei Sigma-Aldrich, abgerufen am 24. April 2011.
- ↑ Nicht explizit in RL 67/548/EWG, Anh. I gelistet, fällt aber dort mit der angegebenen Kennzeichnung unter den Sammelbegriff „Thalliumverbindungen“; Eintrag in der GESTIS-Stoffdatenbank des IFA, abgerufen am 30. März 2009 (JavaScript erforderlich)
- ↑ Thallium Bromoiodide (KRS-5) Optical Crystals. International Crystal Laboratories, abgerufen am 4. Mai 2010.
Weblinks
- Datenblatt von LOT-Oriel-Lasers (PDF-Datei; 86 kB)
- Datenblatt von Korth Kristalle GmbH
- Datenblatt von Saint-Gobain Crystals (englisch) (PDF-Datei; 60 kB)
Kategorien:- Giftiger Stoff
- Umweltgefährlicher Stoff
- Thalliumverbindung
- Iodid
- Bromid
Wikimedia Foundation.
