- Wolfram(VI)-oxid
-
Kristallstruktur 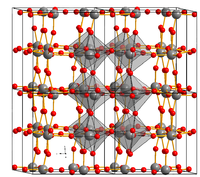
__ W6+ __ O2− Allgemeines Name Wolfram(VI)-oxid Andere Namen Wolframtrioxid
Verhältnisformel WO3 CAS-Nummer 1314-35-8 PubChem 14811 Kurzbeschreibung zitronengelbes Pulver[1]
Eigenschaften Molare Masse 231,85 g·mol−1 Aggregatzustand fest
Dichte Schmelzpunkt Löslichkeit Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [3] 
Achtung
H- und P-Sätze H: 302-315-319-335 EUH: keine EUH-Sätze P: 261-305+351+338 [3] EU-Gefahrstoffkennzeichnung [2] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 22 S: keine S-Sätze Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Wolfram(VI)-oxid, auch Wolframtrioxid (WO3), stellt das wichtigste Oxid des Wolframs dar.
Inhaltsverzeichnis
Vorkommen
Wolfram(VI)-oxid kommt natürlich in Form der Minerale Elsmoreit (Wolfram(VI)-oxid Halbhydrat), Tungstit (Wolfram(VI)-oxid Hydrat) und Meymacit (Wolfram(VI)-oxid Dihydrat) vor.[4]
Herstellung
Die Gewinnung von Wolframtrioxid erfolgt durch Glühen von Wolfram oder Wolframverbindungen unter Luftzutritt.
Eigenschaften
Wolfram(VI)-oxid, ist ein bei Raumtemperatur intensiv gelb gefärbtes, beim Erwärmen orangefarbenes Kristallpulver. Das Kristallgitter des rhombischen WO3 besteht aus WO6-Oktaedern, die in den drei Raumrichtungen über gemeinsame Ecken miteinander verbunden sind. Wolframtrioxid ist in Wasser und Säuren völlig unlöslich, kann aber mit Wasser zu Wolframsäure reagieren. Mit Laugen reagiert es zu Wolframaten.
Verwendung
Wolframtrioxid wird in der Keramikindustrie als Kontakt sowie als Gelbpigment verwendet. Eine gewisse Bedeutung könnte WO3 bei der Herstellung ultradünner Oxidfilme erlangen, mit denen sich optische Linsen kratzfest beschichten lassen. Auch elektrochrome Verglasungen enthalten Wolframtrioxid.
Einzelnachweise
- ↑ a b c Römpp Online - Version 3.5, 2009, Georg Thieme Verlag, Stuttgart.
- ↑ a b c Eintrag zu Wolframtrioxid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 11. November 2007 (JavaScript erforderlich).
- ↑ a b Datenblatt Tungsten(VI) oxide bei Sigma-Aldrich, abgerufen am 25. April 2011.
- ↑ Mineralienatlas: Tungstit
Weblinks
Wikimedia Foundation.

