- Zinn(IV)-oxid
-
Kristallstruktur 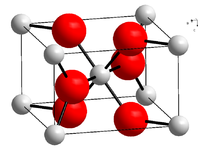
__ Sn4+ __ O2- Allgemeines Name Zinn(IV)-oxid Andere Namen - Zinnasche
- Zinnblüten
- Zinndioxid
- Zinnsäureanhydrid
- Zinnweiß
Verhältnisformel SnO2 CAS-Nummer 18282-10-5 PubChem 29011 Kurzbeschreibung amorphes, weißes Pulver oder hexagonale, tetragonale beziehungsweise rhombische Kristalle[1]
Eigenschaften Molare Masse 150,71 g·mol−1 Aggregatzustand fest
Dichte Schmelzpunkt Löslichkeit - unlöslich in Wasser[1]
- löslich in konzentrierter Salzsäure und Salpetersäure[1]
Sicherheitshinweise EU-Gefahrstoffkennzeichnung [2] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: keine S-Sätze Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Zinn(IV)-oxid, auch Zinndioxid, ist der Hauptbestandteil des Minerals Kassiterit (Zinnstein) und so Hauptquelle der Erzeugung von reinem Zinn.
Inhaltsverzeichnis
Gewinnung und Darstellung
Man kann Zinn(IV)-oxid durch Verbrennung von Zinn an Luft, durch Reaktion von Zinn(IV)-chlorid und Wasser (beides als Dampf) bei hohen Temperaturen, sowie durch Reaktion von Zinn mit Schwefelsäure und anschließend mit Hydroxiden gewinnen.
Chemische Eigenschaften
Das wasserunlösliche, amphotere Zinndioxid löst sich in starken Säuren wie Salzsäure oder Iodwasserstoffsäure unter Bildung von entsprechenden Hexahalogenstannaten:[3][4]
Mit starken Laugen bilden sich die Salze der teils frei nicht existenten Zinnsäuren H2[Sn(OH)6] und H2SnO3 (Metazinn(IV)-säure). Die entsprechenden Alkalisalze wie Na2SnO3 oder Na2[Sn(OH)6] sind stabil und werden, wie etwa das Natriumstannat Na2[Sn(OH)6] in der Färbeindustrie eingesetzt.
Verwendung
Zinn(IV)-oxid wird als Halbleiter (bei Zusatz von Antimonoxid) für die Photovoltaik (siehe auch Grätzel-Zelle), in Lichtleitfasern oder LC-Displays (als transparente elektrisch leitfähige Schicht) und in Gassensoren (reagiert mit Widerstandsveränderung auf alle oxidierbaren Gase oder Dämpfe) verwendet. Weiterhin dient es als Poliermehl für Stahl, Glas und Naturstein, als weißes, durchsichtiges Trübungsmittel bei der Herstellung von Keramikglasuren, Milchglas und Email, zur Versiegelung von Rissen in Glas und als Katalysator bei chemischen Prozessen. Früher diente es als Glasur bei der Herstellung von Fayencen.
Einzelnachweise
- ↑ a b c Zinnoxide in: Römpp Online - Version 3.5, 2009, Georg Thieme Verlag, Stuttgart.
- ↑ a b c Eintrag zu Zinndioxid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 10. November 2007 (JavaScript erforderlich).
- ↑ Donaldson & Grimes: Chemistry of tin ed. P. G. Harrison Blackie (1989).
- ↑ Earle R. Caley: The Action Of Hydriodic Acid On Stannic Oxide. In: J. Am. Chem. Soc., 1932, 54, 8, S. 3240–3243, doi:10.1021/ja01347a028.
Weblinks
Wikimedia Foundation.

![\mathrm{SnO_2 \ + \ 6 \ HI \ \longrightarrow \ \ H_2[SnI_6] \ + \ 2 \ H_2O}](1/6110c43815b3f5880cf07e50a32b30f1.png)

