- MoOPH
-
Strukturformel 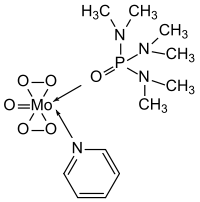
Allgemeines Name MoOPH Andere Namen - Oxodiperoxymolybdän-pyridin-hexamethylphosphoramid
Summenformel C11H23MoN3O6P CAS-Nummer - Eigenschaften Molare Masse 324.29 g·mol−1 Aggregatzustand fest
Schmelzpunkt Sicherheitshinweise EU-Gefahrstoffkennzeichnung [2] keine Einstufung verfügbar R- und S-Sätze R: siehe oben S: siehe oben Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. MoOPH (oder Oxodiperoxymolybdän-pyridin-hexamethylphosphorsäuretriamid) ist ein Molybdänkomplex der von Edwin Vedejs als Reagenz für die Organische Synthese vorgestellt wurde. Der Komplex dient zur Oxidation von Carbanionen.
Inhaltsverzeichnis
Anwendung
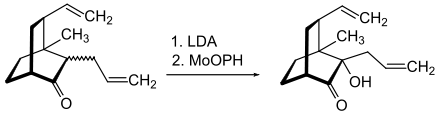
MoOPH ist ein Oxidationsmittel für Carbanionen wie z. B. Enolationen. Im gezeigten Beispiel wird mit Hilfe von Lithiumdiisopropylamid (LDA) ein Enolation erzeugt und durch Umsetzung mit MoOPH zum α-Hydroxyketon (Acyloin) hydroxyliert:[3]
Da das als Ligand verwendete Hexamethylphosphorsäuretriamid (HMPT) als carcinogen eingestuft ist, wurde ein gesundheitlich unbedenklicheres Analogon mit dem Liganden Dimethylpropylenharnstoff (DMPU) eingeführt, das sogenannte MoOPD (Oxodiperoxymolybdän-pyridin-dimethylpropylenharnstoff).[4]
Darstellung
MoOPH wird in einer drei Synthesestufen umfassenden Reaktionsfolge hergestellt. Zunächst wird das Molybdän(VI)-oxid zum Diperoxid oxidiert und mit Hexamethylphosphorsäuretriamid (HMPT) zum Hydrato-Komplex umgesetzt. Ein Trocknungsschritt entfernt das Wasser als Liganden. Der so erhaltene Komplex wird mit Pyridin zum MoOPH umgesetzt, welches als gelbes Pulver erhalten wird.[1]
Literatur
- Bang-Chi Chen, Ping Zhou, Franklin A. Davis, Engelbert Cianek: "α-Hydroxylation of Enolates and Silyl Enol Ethers", In: Organic Reaktions, Wiley 2004 doi:10.1002/0471264180.or062.01.
Einzelnachweise
- ↑ a b Edwin Vedejs, S. Larsen: Organic Syntheses, Coll. Vol. 7, p.277 (1990) Online Version
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Dietrich Spitzner, Kai Oesterreich: "Anionically Induced Domino Reactions − Synthesis of a Norpatchoulenol-Type Terpene", in: European Journal of Organic Chemistry, 2001, 10, 1883-1886 doi:10.1002/1099-0690(200105)2001:10<1883::AID-EJOC1883>3.0.CO;2-M
- ↑ J.C. Anderson, S.C. Smith: in Synlett 1990, 107–108.
Wikimedia Foundation.

![\mathrm{MoO_3 \xrightarrow[2. HMPT] {1. H_2O_2} MoO_5 (H_2O) [(Me_2N)_3PO]}](0/a0073fe35108e7d04362aefdb3fcfa8f.png)
![\mathrm{\xrightarrow{0.2 Torr} MoO_5 [(Me_2N)_3PO]}](8/6a81974c8c845e59a41c46a4fbcdf5f4.png)
}](4/4741a125d1a57afdeacbea58cc89d4e5.png)