- Molybdän(VI)-oxid
-
Kristallstruktur 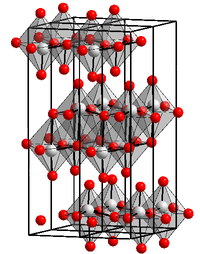
__ Mo6+ __ O2- Kristallsystem orthorhombisch[1]
Raumgruppe Pbnm[1]
Gitterkonstanten Allgemeines Name Molybdän(VI)-oxid Andere Namen - Molybdäntrioxid
- Molybdänsäureanhydrid
- Wasserbleierde
Verhältnisformel MoO3 CAS-Nummer 1313-27-5 PubChem 14802 Kurzbeschreibung gelblichgrüner, geruchloser Feststoff[2]
Eigenschaften Molare Masse 143,93 g·mol−1 Aggregatzustand fest
Dichte 4,70 g·cm−3[2]
Schmelzpunkt Siedepunkt 1155 °C[2]
Löslichkeit schlecht in Wasser (0,5 g·l−1 bei 20 °C)[2]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [3] 

Achtung
H- und P-Sätze H: 351-319-335 EUH: keine EUH-Sätze P: 281-305+351+338-308+313 [2] EU-Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [3] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 36/37-40 S: (2)-22-36/37 MAK aufgehoben, da cancerogen[2]
LD50 125 mg·kg−1 (Ratte, oral)[4]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Molybdän(VI)-oxid ist eine pulverförmige weiße Verbindung, die beim Rösten vieler Molybdänverbindungen zurückbleibt.
Inhaltsverzeichnis
Geschichte
1778 gelang es Carl Wilhelm Scheele aus Molybdänglanz durch Behandlung mit Salpetersäure Molybdän(VI)-oxid herzustellen. 1782 reduzierte Peter Jacob Hjelm das Oxid mit Kohle zum elementaren Molybdän.
Vorkommen
In der Natur kommt es in Form des seltenen Minerals Molybdit vor.
Gewinnung und Darstellung
Molybdän(VI)-oxid wird industriell durch Oxidation von Molybdän(IV)-sulfid gewonnen:
Im Labor kann es auch durch Reaktion von Ammoniumheptamolybdat und Salpetersäure[1] bzw. aus Natriummolybdat und Perchlorsäure gewonnen, wobei jeweils Molybdän(VI)-oxid-dihydrat entsteht:[5]
Das entstehende Dihydrat wandelt sich leicht in das Monohydrat um. Beide Hydrate haben eine hellgelbe bis gelblichgrüne Farbe. Oberhalb von 450 °C setzten sich diese zum Anhydrid um.
Eigenschaften
Molybdän(VI)-oxid liegt als weißes Pulver vor, das sich beim Erhitzen gelb färbt und nach dem Erkalten wieder farblos wird. Es hat die Verhältnisformel MoO3, einen Schmelzpunkt von 795 °C und einen Siedepunkt von 1155 °C. Molybdän(VI)-oxid ist in Wasser schwerlöslich, geht jedoch in alkalischer Lösung in Molybdat-Ionen MoO42− über. In verdünnter Lösung kann man dieses durch Ansäuern in die Molybdänsäure H2MoO4 überführen.
Es hat einen relativ hohen Dampfdruck. Es sublimiert deshalb ab ca. 700 °C merklich, wobei sich glänzende, leicht grünliche, kristalline Flitter bilden.

Molybdän(VI)-oxid besitzt eine orthorhombische Kristallstruktur. Es besteht aus Schichten von verzerrten MoO6-Oktaedern in einem orthorhombischen Kristall. Die Oktaeder sind an den Kanten verbunden und bilden Ketten, die über Sauerstoff-Atome verbunden sind und Schichten bilden.
Verwendung
Molybdän(VI)-oxid ist der Ausgangsstoff für die Synthese der meisten anderen Molybdänverbindungen, es dient als Emaillezusatz und zur Herstellung von reinem Molybdän (z. B. durch Reduktion mit Wasserstoff).
Es ist auch ein Katalysator (Molybdäntrioxid-Pulver auf Aluminiumoxid) für Hydroformier-, Alkylierungs-, Entschwefelungs- und Krackprozesse in der Petrochemie und bei der Herstellung von Acrylnitril.
Molybdän(VI)-oxid verfügt über eine antimikrobielle Wirkung. In Kontakt mit Wasser bilden sich Hydronium-Ionen, welche die Keime durch Absenkung des pH-Wertes zerstören. Diese Eigenschaft macht die Substanz interessant zur Desinfektion, insbesondere im Krankenhausbereich.
Siehe auch
- Molybdän(II)-oxid MoO, CAS: 12058-07-0
- Molybdän(IV)-oxid MoO2, CAS: 18868-43-4
- Molybdän(VI)-oxidtetrachlorid MoOCl4, CAS: 13814-75-0
Einzelnachweise
- ↑ a b c d e f Brauer, Handbuch der Präparativen Anorganischen Chemie
- ↑ a b c d e f g Eintrag zu Molybdän(VI)-oxid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3.9.2007 (JavaScript erforderlich)
- ↑ a b Eintrag zu CAS-Nr. 1313-27-5 im European chemical Substances Information System ESIS (ergänzender Eintrag)
- ↑ ScienceLab: MSDS
- ↑ Heynes, J. B. B.; Cruywagen, J. J. "Yellow Molybdenum(VI) Oxide Dihydrate" Inorganic Syntheses, 1986, volume 24, pp. 191. ISBN 0-471-83441-6.
Kategorien:- Stoff mit Verdacht auf krebserzeugende Wirkung
- Oxid
- Molybdänverbindung
- Katalysator
Wikimedia Foundation.



