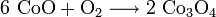- CoO*Co2O3
-
Kristallstruktur Keine Kristallstruktur vorhanden Allgemeines Name Cobalt(II,III)-oxid Andere Namen Tricobalttetraoxid
Verhältnisformel Co3O4 CAS-Nummer 1308-06-1 Kurzbeschreibung schwarzer Feststoff Eigenschaften Molare Masse 240,8 g·mol−1 Aggregatzustand fest
Dichte 6,07 g·cm−3[1]
Schmelzpunkt 895 °C [1]
Siedepunkt >900 °C (Zersetzung)[1]
Löslichkeit unlöslich in Wasser[1]
Sicherheitshinweise Gefahrstoffkennzeichnung [1] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 40-43 S: 36/37 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Cobalt(II,III)-oxid in eine chemische Verbindung von Cobalt und Sauerstoff. Der schwarze Feststoff ist eines vom mehreren Oxiden des Cobalts.
Inhaltsverzeichnis
Gewinnung und Darstellung
Cobalt(II,III)-oxid entsteht beim Erhitzen von Cobalt(II)-oxid an der Luft auf 400 bis 500 °C.[2]
Eigenschaften
Cobalt(II,III)-oxid ist eine gemischtvalente Verbindung mit zwei- und dreiwertigen Cobaltionen und der genaueren Formel Co2+Co3+2O4 (CoO*Co2O3). Die Verbindung besitzt eine Spinellstruktur, bei der in einer kubisch dichtesten Kugelpackung von O2--Ionen ein Achtel aller Tetraederlücken und die Hälfte der Oktaederlücken von Cobaltionen besetzt sind. Die Co2+-Ionen besetzen dabei die Tetraederlücken, die Co3+-Ionen die Oktaederlücken.[2]
Ab etwa 900 °C zersetzt sich Cobalt(II,III)-oxid zu Cobalt(II)-oxid. Von Reduktionsmitteln wie Koks oder Aluminium wird die Verbindung zu elementarem Cobalt reduziert.[2]
Verwendung
Cobalt(II,III)-oxid ist ein wichtiges Zwischenprodukt bei der Gewinnung von metallischen Cobalt. Durch Rösten und Auslaugen wird aus verschiedenen Cobalterzen (meist Sulfide oder Arsenide) zunächst Cobalt(II,III)-oxid gewonnen. Dieses kann nun mit Kohlenstoff oder aluminothermisch zum Element reduziert werden.[2]
Cobalt(II,III)-oxid lässt sich als Katalysator zur Oxidation von Ammoniak zu Salpetersäure einsetzen. Dieses ist deutlich billiger als die sonst verwendeten Platin-Legierungen. Ein Nachteil ist allerdings die bisher geringere Selektivität von Cobalt(II,III)-oxid-Katalysatoren.[3]
Wie andere Cobaltverbindungen ist Cobalt(II,III)-oxid ein Blaupigment für das Färben von Keramiken.[4]
Sicherheitshinweise
Cobalt(II,III)-oxid wird als Krebserregend und Keimzellmutagen angesehen.[1]
Einzelnachweise
- ↑ a b c d e f Eintrag zu Cobalt(II,III)-oxid in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 15.11.2008 (JavaScript erforderlich)
- ↑ a b c d Arnold F. Holleman, Nils Wiberg: Lehrbuch der Anorganischen Chemie, 102. Auflage, de Gruyter, Berlin 2007, S. 1682-87, ISBN 978-3-11-017770-1.
- ↑ Poul Erik Hojlund Nielsen, Keld Johansen: Ammonia oxidation catalyst. EP19930104797, 1993.
- ↑ Rohstoffübersicht Keramik, Fa. Lehrer
Wikimedia Foundation.