- Acetylcystein
-
Strukturformel 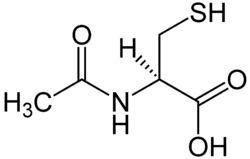
Allgemeines Freiname Acetylcystein Andere Namen - L-α-Acetamido-β-mercaptoproprionsäure
- (R)-2-Acetylamino-3-sulfanylpropansäure
- ACC
- N-Acetylcystein (NAC)
- (R)-N-Acetylcystein
- L-N-Acetylcystein
Summenformel C5H9NO3S CAS-Nummer 616-91-1 PubChem 12035 ATC-Code Kurzbeschreibung Weißer kristalliner Feststoff [1]
Arzneistoffangaben Wirkstoffklasse Wirkmechanismus Spaltung der Disulfidbrücken des Sekrets in den Bronchien
Verschreibungspflichtig: Ja (teilweise) Eigenschaften Molare Masse 163,20 g·mol−1 Aggregatzustand fest
Schmelzpunkt Sicherheitshinweise Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln GHS-Gefahrstoffkennzeichnung [1] keine GHS-Piktogramme H- und P-Sätze H: keine H-Sätze EUH: keine EUH-Sätze P: keine P-Sätze [1] EU-Gefahrstoffkennzeichnung [1] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: 22-24/25 LD50 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Acetylcystein (abgekürzt ACC, NAC; veraltet Mercaptursäure) ist ein Arzneistoff, der als Expektorans (zur Schleimlösung) bei Atemwegserkrankungen mit festsitzendem Auswurf, wie etwa bei einer Bronchitis, eingesetzt wird. Der in den Bronchien festsitzende zähe Schleim kann nach einer Verflüssigung (Sekretolyse) besser abgehustet werden.
Neben der medizinischen Verwendung in Arzneimitteln wird Acetylcystein als Bestandteil diätetischer Lebensmittel eingesetzt,[2] die außerhalb von Apotheken auch in Drogerien erhältlich sind.
Derivate des N-Acetyl-L-cysteins sind Abbauprodukte der Kondensationsprodukte von Glutathion mit Fremdstoffen im menschlichen Körper (im Rahmen der Biotransformation) und können im Urin nachgewiesen werden.
Inhaltsverzeichnis
Sekretolytische Wirkung
Die schleimverflüssigende Wirkung soll durch Spaltung der Disulfidbrücken der Mucopolysaccharidfasern, aus denen das in den Bronchien gebildete Sekret besteht, zustande kommen. Ein alternativer Wirkungsmechanismus soll auf der Fähigkeit der reaktiven SH-Gruppe von Acetylcystein beruhen, chemische Radikale zu binden und dadurch entzündungshemmend zu wirken.
Der Wirkstoff Acetylcystein hat sich in präklinischen Studien als untoxisch erwiesen.[3][4] So führte beispielsweise die perorale Gabe von 300 mg/kg des Wirkstoffs über 52 Wochen bei Hunden zu keinerlei gesundheitlichen Veränderungen.[5] In einer klinischen Studie am Menschen zeigte sich, dass eine Tagesdosis von 11,6 g N-Acetylcystein oral über einen Zeitraum von drei Monaten zu keinen schwerwiegenden Nebenwirkungen führt.[6]
Die therapeutische Wirksamkeit bei Bronchitis ist umstritten, da die aus den 1980er Jahren stammenden Studien heutigen Ansprüchen an ein Studiendesign nicht standhalten.[7] Bei cystischer Fibrose scheinen hohe Dosen von Acetylcystein jedoch eine Besserung der Verschleimung zu bewirken.[8]
Es wird auch zur Vermeidung von Rezidiven nach der Operation einer Dupuytrenschen Kontraktur eingesetzt. Hier wird ebenfalls auf die Wirkung gegen fibrotische Veränderungen gesetzt.
Anwendung als Antidot
Unbestritten ist hingegen der Einsatz von Acetylcystein bei akuten Paracetamol-Überdosierungen, bei denen es Leberschäden abwenden oder abschwächen kann. In diesem Fall wird ACC für 72 Stunden oral oder 20 bis 21 Stunden intravenös gegeben. Dabei ist die orale Gabe genauso wirksam wie die intravenöse, aber schlechter verträglich (Übelkeit und Erbrechen). Zumindest in Europa wird deshalb die intravenöse Gabe bevorzugt. Am effektivsten ist die Therapie, wenn sie in weniger als acht Stunden nach Paracetamolaufnahme begonnen wird. Auch in allen Phasen der Schwangerschaft wird ACC als Antidot empfohlen. Acetylcystein stellt dem Körper Cystein zur Verfügung, welches er zur Bildung von Glutathion benötigt. Glutathion spielt eine wichtige Rolle in der Biotransformation schädlicher Substanzen („Entgiftung“). Speziell beim Abbau von Paracetamol durch Cytochrom P450 entsteht N-Acetyl-p-benzochinonimin, welches Leberzellen zerstört und durch Glutathion neutralisiert wird.[9][10][11][12][13][14]
Anwendung außerhalb zugelassener Anwendungsgebiete
Auch bei der Vorbeugung des akuten Nierenversagens bei Risikopatienten vor Röntgenverfahren mit Kontrastmitteln kommt Acetylcystein zum Einsatz. Hier werden jeweils 2 × 600 mg am Tag vor der Untersuchung und am Untersuchungstag gegeben. Die Wirksamkeit dieser Maßnahme ist umstritten. Während einige wenige Studien eine hohe Wirksamkeit der Acetylcystein-Prophylaxe fanden, zeigte sich in der Mehrzahl der Untersuchungen kein signifikanter Effekt.[15]
In Tierversuchen an Mäusen hat sich gezeigt, dass ACC die Überlebensrate nach einer Infektion mit Malaria-Erregern – Parasiten der Gattung Plasmodium – von 20 auf 100 Prozent steigert. Der Körper wird in die Lage versetzt, die Leberzellen vor einem Überschuss an freiem Häm zu schützen, das bei der Zerstörung roter Blutkörperchen ins Blut abgegeben wird. Ob der Wirkstoff auch bei einer Malaria-Erkrankung des Menschen hilft, ist bis jetzt noch nicht durch Studien erwiesen.[16][17]
Der Einsatz von Acetylcystein bei HIV- und AIDS-Patienten wurde bereits in kleinen Studien untersucht. Bisher wurden keine signifikanten Auswirkungen einer ACC-Behandlung auf die Surrogatmarker des HIV-Krankheitsverlaufes wie Viruslast oder Anzahl der CD4-Zellen nachgewiesen. Eine Stellungnahme der Fachgesellschaften und eine offizielle Therapieempfehlung zu Acetylcystein existiert bisher nicht.
Literatur
- T. Ahola, V. Fellman, R. Laaksonen, J. Laitila, R. Lapatto, P. J. Neuvonen, K. O. Raivio: Pharmacokinetics of intravenous N-acetylcysteine in pre-term new-born infants. In: Eur J Clin Pharmacol 55, 1999, S. 645–650.
- G. K. Isbister, I. K. Bucens, I. M. Whyte: Paracetamol overdose in a preterm neonate. In: Arch Dis Child Fetal Neonatal Ed. 85, 2001, S. F70-2.
Einzelnachweise
- ↑ a b c d e f Datenblatt N-Acetyl-L-cysteine bei Sigma-Aldrich, abgerufen am 20. März 2011.
- ↑ siehe Anlage 2 zu den §§ 7, 7a und 7b der Verordnung über diätetische Lebensmittel (Diätverordnung).
- ↑ D. C. Plumb: Veterinary Drug Handbook. PharmaVet Publishing, White Bear Lake (USA); 853 Seiten, 1999.
- ↑ R. E. Johnston, H. C. Hawkins, J. H. Weikel Jr.: The toxicity of N-acetylcysteine in laboratory animals. In: Semin Oncol 10 Suppl 1: 1983, S. 17–24.
- ↑ H. Keller, A. Faulstich, M. Elker, M. Grell, S. Wuschko, J. H. Rehders: Klinische Studie zur Wirksamkeit und Verträglichkeit von N-Acetylcystein bei der Behandlung der COB/COPD des Pferdes. In: Prakt Tierarzt 82(2): 2001, S. 108–117.
- ↑ Muster.
- ↑ Arzneiverordnung in der Praxis. Band 33, 3. Ausgabe, Juli 2006.
- ↑ R. Tirouvanziam u.a.: High-dose oral N-acetylcysteine, a glutathione prodrug, modulates inflammation in cystic fibrosis. In: PNAS 103, 2006, S. 4628–4633. PMID 16537378.
- ↑ H. Kupferschmidt:Therapie der Paracetamolvergiftung (Schweizerisches Toxikologisches Informationszentrum)
- ↑ M. J. Smilkstein, G. L. Knapp, K. W. Kulig, B. H. Rumack: Efficacy of oral N-acetylcysteine in the treatment of acetaminophen overdose. Analysis of the national multicenter study (1976 to 1985). In: N. Engl. J. Med.. 319, Nr. 24, Dezember 1988, S. 1557–1562. PMID 3059186.
- ↑ L. F. Prescott, J. Park, A. Ballantyne, P. Adriaenssens, A. T. Proudfoot: Treatment of paracetamol (acetaminophen) poisoning with N-acetylcysteine. In: Lancet. 2, Nr. 8035, August 1977, S. 432–434. PMID 70646.
- ↑ E. Kozer, G. Koren: Management of paracetamol overdose: current controversies. In: Drug Saf. 24, Nr. 7, 2001, S. 503–12. PMID 11444723.
- ↑ B. Bailey: Are there teratogenic risks associated with antidotes used in the acute management of poisoned pregnant women?. In: Birth Defects Res. Part A Clin. Mol. Teratol.. 67, Nr. 2, Februar 2003, S. 133–140. doi:10.1002/bdra.10007. PMID 12769509.
- ↑ Richard Dekhuijzen: N-Acetylcysteine and cytoprotective effects against bronchopulmonary damage: from in vitro studies to clinical application. In: Roberta Masella, Giuseppe Mazza (Hrsg.): Glutathione and Sulfur Amino Acids in Human Health and Disease. Wiley, 2009, ISBN 0-470-17085-9, S. 519-542.
- ↑ Fishbane, Steven: N-Acetylcysteine in the Prevention of Contrast-Induced Nephropathy. In: Clin J Am Soc Nephrol. Nr. 3, 2008, S. 281-287 (Link frei ab Januar 2009 ArtikelAbstract).
- ↑ E. Seixas, R. Gozzelino, A. Chora, u.a.:: Heme oxygenase-1 affords protection against noncerebral forms of severe malaria. In: PNAS. 106, Nr. 37, September 2009, S. 15837–15842. doi:10.1073/pnas.0903419106. PMID 19706490. Volltext bei PMC: 2728109.
- ↑ wissenschaft.de: Mit Hustenlöser gegen Malaria. Zugriff am 5. Juli 2010.
Handelsnamen
ACC (D, A, CH), Acemuc (D), Acemucol (CH), Acetyst (D), Aeromuc (A), Dynamucil (CH), Fluimucil (D, A, CH), Helvetussin (CH), Mucobene (A), Mucofluid (CH), Myxofat (D), NAC (D), Secresol (CH), Solmucol (CH), diverse Generika (D, CH)
Alvesin (D), Aminopäd (D), Aminoplasmal (D), Deltamin (D), Infesol (D), Nephrotec (D), Periplasmal (D, A), Pädamin (A), Rinofluimucil (CH), Salviamin (D), Solmucalm (CH),
Weblinks

Bitte den Hinweis zu Gesundheitsthemen beachten! Kategorien:- ATC-R05
- ATC-V03
- ATC-S01
- Expektorans
- Antidot
- Carbonsäureamid
- Carbonsäure
- Thiol
- Arzneistoff
- Antioxidationsmittel
Wikimedia Foundation.
