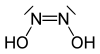
- Hyposalpetrige Säure
-
Strukturformel 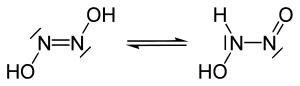
Allgemeines Name - Hyposalpetrige Säure
Andere Namen - Untersalpetrige Säure
- Diazendiol
- Hyposalpetrigsäure
Summenformel H2N2O2 CAS-Nummer 14448-38-5 PubChem 61744 Kurzbeschreibung farblose, im trockenen Zustand explosive Plättchen[1]
Eigenschaften Molare Masse 62,0 g·mol−1 Aggregatzustand fest
pKs-Wert Löslichkeit Sicherheitshinweise EU-Gefahrstoffkennzeichnung [3] keine Einstufung verfügbar R- und S-Sätze R: siehe oben S: siehe oben Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Hyposalpetrige Säure ist eine Sauerstoffsäure des Stickstoff. Sie bildet farblose Kristalle, die explosiv sind. Diese sind löslich in Ethanol und Wasser.
Es existieren eine cis- und eine stabilere trans-Hyposalpetrige Säure.
Von der cis-Form sind nur die Salze bekannt; die trans-From lässt sich in Substanz isolieren.[2]
Ihre Salze heißen Hyponitrite, z. B.: Kaliumhyponitrit (K2N2O2).
Herstellung
trans-Hyposalpetrige Säure kann durch Reduktion von Salpetriger Säure oder Natriumnitrit mit nascierendem Wasserstoff (z. B. aus Natrium-Amalgam) hergestellt werden.[2][4]
Das wasserlösliche Natriumsalz kann mit Silbernitrat als gelbes, unlösliches Silberhyponitrit abgetrennt werden:
Nach dem Abtrennen kann die trans-Hyposalpetrige Säure mit HCl-Gas in Ether wieder gelöst werden:
Reaktionen
Mit Alkalimetallen bildet die Hyposalpetrige Säure Salze, die Hyponitrite:
Die schwach saure wässrige Lösung der Säure zerfällt bereits bei Zimmertemperatur zu Distickstoffmonoxid und Wasser:
Die Reaktion ist nicht umkehrbar; Distickstoffmonoxid ist also nicht das Anhydrid der hyposalpetrigen Säure.[2]
Sie eignet sich auch als Reaktionspartner für Hetero-Diels-Alder-Reaktionen.[5]
Einzelnachweise
- ↑ a b Thieme Chemistry (Hrsg.): RÖMPP Online - Version 3.5. Georg Thieme Verlag KG, Stuttgart 2009.
- ↑ a b c d e A.F.Holleman, E.Wiberg. Lehrbuch der Anorganischen Chemie. Walter de Gruyter & Co. Berlin 1995, 101. Auflage, ISBN 3-11-012641-9.
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry 2nd ed., vol. 1, Academic Press 1963, S. 492-6.
- ↑ Roempp Online.
Kategorien:- Anorganische Säure
- Stickstoffverbindung
Wikimedia Foundation.