- Aluminiumfluorid
-
Kristallstruktur 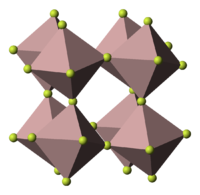
Allgemeines Name Aluminiumfluorid Andere Namen - Aluminiumtrifluorid
- Aluminium(III)-trifluorid
Verhältnisformel AlF3 CAS-Nummer - 7784-18-1
- 32287-65-3 (monohydrat)
- 15098-87-0 (trihydrat)
PubChem 2124 Kurzbeschreibung farblose hexagonale Kristalle[1]
Eigenschaften Molare Masse 83,98 g·mol−1 Aggregatzustand fest
Dichte 2,88 g·cm−3[2]
Sublimationspunkt Löslichkeit schlecht löslich in Wasser, Säuren und Laugen[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [3] 
Achtung
H- und P-Sätze H: 302-315-319-335 EUH: keine EUH-Sätze P: 261-305+351+338 [3] EU-Gefahrstoffkennzeichnung [2] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 22-36/37/38 S: 26 MAK 1 mg·m−3 (gemessen als einatembarer Aerosolanteil)[2]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Aluminiumfluorid ist ein Salz von Aluminium und Fluor mit der Summenformel AlF3.
Inhaltsverzeichnis
Vorkommen
Aluminiumfluorid kommt sowohl wasserfrei, als auch in mehreren kristallwasserhaltigen Formen vor.
Synthese
Die Darstellung von Aluminiumfluorid erfolgt zweckmäßig durch das Überleiten von Fluorwasserstoff über rotglühendes Aluminiumoxid:
Die Dehydrierung des Trihydrats ist allerdings nie ganz frei von der Produktion des Oxids. Um daher reines wasserfreies Aluminiumfluorid herzustellen, greift man auf die Zersetzung von Ammoniumhexafluoroaluminat zurück:[4]
Eigenschaften
Aluminiumfluorid bildet ein in Wasser und organischen Lösungsmitteln schwer lösliches, farbloses triklines Kristallpulver.
Reaktionsverhalten
Mit Fluoriden der Alkalimetalle werden Komplexsalze der Zusammensetzungen M(AlF4), M2(AlF5) sowie M3(AlF6) gebildet.[1] Von technischer Bedeutung ist hierbei Kryolith Na3[AlF6].
Verwendung
Aluminiumfluorid wird als Katalysator, der Zahnpflege zur Kariesprophylaxe, in Form von Kryolith wird es als Flussmittel, zum Schmelzen von Leichtmetallen und zur Herstellung von Aluminium verwendet.[2]
Einzelnachweise
- ↑ a b c Almut Barwinski, in: Roempp Online - Version 3.5, 2009, Georg Thieme Verlag, Stuttgart.
- ↑ a b c d e Eintrag zu Aluminiumfluorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 23. Dezember 2007 (JavaScript erforderlich).
- ↑ a b Datenblatt Aluminum fluoride bei Sigma-Aldrich, abgerufen am 20. März 2011.
- ↑ G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry 2nd ed., vol. 1, Academic Press 1963, S. 225–226.
Kategorien:- Gesundheitsschädlicher Stoff
- Aluminiumverbindung
- Fluorid
Wikimedia Foundation.


