- Fluorwasserstoff
-
Strukturformel 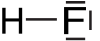
Allgemeines Name Fluorwasserstoff Andere Namen - Hydrogenfluorid
- Fluorwasserstoffgas
- Fluoran
Summenformel HF CAS-Nummer 7664-39-3 PubChem 14917 Kurzbeschreibung farbloses Gas mit stechendem Geruch[1]
Eigenschaften Molare Masse 20,00 g·mol−1 Aggregatzustand gasförmig
Dichte Schmelzpunkt Siedepunkt 19,5 °C[3]
Dampfdruck pKs-Wert 3,2[4]
Löslichkeit mischbar mit Wasser[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [1] 

Gefahr
H- und P-Sätze H: 330-310-300-314 EUH: keine EUH-Sätze P: 260-264-280-284-301+310-302+350 [1] EU-Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [5] 

Sehr giftig Ätzend (T+) (C) R- und S-Sätze R: 26/27/28-35 S: (1/2)-7/9-26-36/37/39-45 MAK 0,83 mg·m−3[1]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Fluorwasserstoff ist ein anorganisch-chemischer Stoff und gehört zu den Halogenwasserstoffen. Bei Zimmertemperatur liegt es als farbloses, stechend riechendes Gas vor, das leichter als Luft ist. Es ist hygroskopisch und dehydratisiert viele Stoffe. In der wasserfreien Form liegt es unterhalb des Siedepunktes von 19,51 °C als rauchende Flüssigkeit vor.
Fluorwasserstoff ist in jedem Verhältnis mit Wasser mischbar und reagiert dabei sauer. Die wässrige Lösung ist als Fluorwasserstoffsäure oder Flusssäure bekannt.
Entdeckt wurde die Fluorwasserstoff-Synthese aus den Elementen durch Henri Moissan.
Inhaltsverzeichnis
Gewinnung und Darstellung
Heutzutage wird Fluorwasserstoff durch die Reaktion seiner Salze, den Fluoriden (Beispiel: Calciumfluorid, Flussspat), mit konzentrierter Schwefelsäure hergestellt:
Anwendung findet diese Reaktion auch beim Nachweis von Fluoriden mittels der Kriechprobe.
Achtung: Aufgrund der hohen Giftigkeit von Fluorwasserstoff sollten alle Versuche, bei denen dieser auch nur in geringsten Mengen freigesetzt wird, im Abzug durchgeführt werden!
Fluorwasserstoff fällt außerdem bei der Aluminiumherstellung und beim Brennen von Ziegeln und Feinkeramik an. Weiterhin wird es bei der Verbrennung von fluorhaltigen Abfällen oder Brennstoffen wie beispielsweise Steinkohle freigesetzt.
Eigenschaften
Physikalische Eigenschaften
- Kritische Temperatur: 188 °C[1]
- Kritischer Druck: 6,49 MPa[1]
- Kritische Dichte: 0,29 g·cm−3[1]
- Molares Normvolumen: 21,7 l/mol
Chemische Eigenschaften
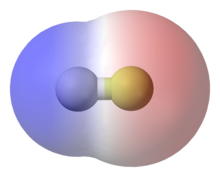
Das chemische Verhalten des Fluorwasserstoffs wird geprägt durch die extrem hohe Elektronegativität des Fluors, welches mit 4 (Pauling-Skala) die höchste aller Elemente aufweist. Das Fluorwasserstoffmolekül ist gekennzeichnet durch einen ausgeprägten Dipolcharakter mit starker negativer Partialladung beim Fluor. Durch Wasserstoffbrücken bilden sich Oligomere wie etwa (HF)6. HF hat im Vergleich zu seinem höheren analogen HCl einen relativ hohen Siedepunkt von 19,5 °C; HCl siedet demgegenüber bei −85,0 °C. Dieses Phänomen ist – wie beim Wasser – auf die gebildeten Wasserstoffbrücken-Bindungen zurückzuführen.
Wässrige HF-Lösung, die Flusssäure, ist eine schwache Säure; jedoch ist wasserfreier Fluorwasserstoff eine sehr starke Protonsäure und autoprotolysiert folgendermaßen:
Fluorwasserstoff ätzt Glas und reagiert mit anderen Silikaten zu gasförmigem Siliciumtetrafluorid:
Fluorwasserstoff zeigt innerhalb der Reihe der Halogenwasserstoffe die schwächste Neigung zur Dissoziation in Wasser. Gegenüber den übrigen Halogenwasserstoffen, die vollständig dissoziieren unter Bildung von Oxonium-Ionen (H3O+) und ihrer entsprechenden Gegenionen, liegt in der Flusssäure ein Gemisch verschiedener fluoridhaltiger Ionen vor.
Reiner gasförmiger Fluorwasserstoff kann in Tankwaggons aus Eisen transportiert werden, da sich die Oberfläche des Eisens mit einer Fluoridschicht überzieht, die das Material gegen weiteren Angriff passiviert. Für Ventile, Rohrleitungen und Apparaturen wird auch Monelmetall (eine Nickel-Kupfer-Legierung) verwendet. Die wässrigen Lösungen dagegen würden das Eisen aufgrund des Anlösens der Fluoridschicht tiefgreifend oxidieren. Daher wird Flusssäure in Kunststoff-Tanks transportiert.
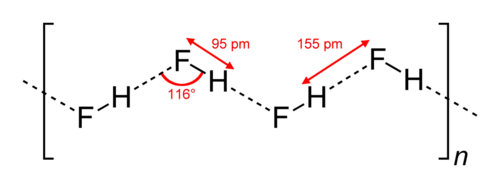
Fluorwasserstoff als Feststoff besteht aus orthorhombischen Kristallen mit Ketten, die im Zick-Zack-Muster angeordnet sind. Die HF-Moleküle haben eine H–F-Bindungslänge von 95 pm, die benachbarten Moleküle haben einen intermolekularen H–F-Abstand von 155 pm.[6]
Verwendung
Fluorwasserstoff findet Verwendung bei der Herstellung von Fluorkohlenwasserstoffen, Aluminiumfluorid, synthetischem Kryolith (Eisstein, Na3[AlF6]), Uranhexafluorid, anderen Fluorverbindungen, Flusssäure, beim Herstellungsprozess von Tensiden und in der Farbstoffchemie. Bei der Elektrolyse von Fluorwasserstoff entsteht unter bestimmten Bedingungen elementares Fluor (F2).
Fluorwasserstoff wird als Katalysator bei der Benzinherstellung, als Lösungsmittel, in der organischen Chemie für die Substitution mit Fluor und in der Tieftemperaturtechnik eingesetzt.
Biologische Bedeutung
Der Hauptaufnahmeweg für Fluorwasserstoff verläuft über die Atemwege und über die Haut. Aufgrund der hohen Hygroskopizität dürfte es nur in Extremfällen zum Einatmen von gasförmigem Fluorwasserstoff kommen, bei der aber mit nahezu vollständiger Resorption in den oberen Atemwegen zu rechnen ist. Viel häufiger tritt die Resorption von wässrigen Lösungen von Fluorwasserstoff (Fluorwasserstoffsäure oder Flusssäure) über die Haut auf. Die Haut stellt bei der Aufnahme kein Hindernis dar. Mit einer versehentlichen oralen Aufnahme ist aus physikalisch-chemischen Gründen und wegen des äußerst stechenden Geruches nicht zu rechnen. Wässrige Lösungen werden vollständig resorbiert. Der Vorgang kann durch eventuellen Mageninhalt verlangsamt werden.
Kontakt mit Fluorwasserstoff hat akut stark ätzende Wirkung auf Haut und Schleimhäute, insbesondere des Auges. Durch Aufnahme in den Organismus kommt es zur erheblichen Beeinflussung biochemischer Stoffwechselvorgänge durch Enzymhemmung. Chronische Auswirkungen umfassen die Schädigung des Skeletts und der Haut, sowie Beeinträchtigung der Lungenfunktion.
Einzelnachweise
- ↑ a b c d e f g h i Eintrag zu Fluorwasserstoff in der GESTIS-Stoffdatenbank des IFA, abgerufen am 27. Januar 2008 (JavaScript erforderlich).
- ↑ BG Chemie Merkblatt M005 Fluorwasserstoff, Flusssäure und anorganische Fluoride, Ausgabe 8/2009 Jedermann-Verlag Heidelberg, S. 8
- ↑ a b c Sicherheitsdatenblatt (Linde)
- ↑ Arnold F. Holleman, Nils Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Berlin 2007, ISBN 978-3-11-017770-1.
- ↑ Eintrag zu CAS-Nr. 7664-39-3 im European chemical Substances Information System ESIS
- ↑ Johnson, M. W.; Sándor, E.; Arzi, E. The Crystal Structure of Deuterium Fluoride, Acta Crystallographica, 1975, B31, S. 1998–2003. doi:10.1107/S0567740875006711.
Halogenwasserstoffe und zugehörige SäurenHalogenwasserstoffe: Fluorwasserstoff | Chlorwasserstoff | Bromwasserstoff | Iodwasserstoff | Astatwasserstoff
Halogenwasserstoffsäuren: Flusssäure | Salzsäure | Bromwasserstoffsäure | Iodwasserstoffsäure
Wikimedia Foundation.
Schlagen Sie auch in anderen Wörterbüchern nach:
Fluorwasserstoff — (Fluorwasserstoffsäure, Flußsäure HFl) (Mol. Gew. 20, spez. Gew. 0,9879 bei 15° C.), bildet bei niedriger Temperatur eine farblose Flüssigkeit, deren Siedepunkt bei 19,5° und deren Erstarrungspunkt bei –102,5° liegt. Sie wird wie die… … Lexikon der gesamten Technik
Fluorwasserstoff — Flu|or|wạs|ser|stoff 〈m. 1; Chem.〉 farbloses, stechend riechendes Gas, als wässerige Lösung Flusssäure od. Fluorwasserstoffsäure genannt * * * Flu|or|was|ser|stoff; Syn.: (systematisch:) Fluoran, (internat. empfohlen:) Hydrogenfluorid: HF;… … Universal-Lexikon
Fluor — Eigenschaften … Deutsch Wikipedia
Fluorchemie — Eigenschaften … Deutsch Wikipedia
Hydrogenfluorid — Strukturformel Allgemeines Name Fluorwasserstoff Andere Namen Hydrogenf … Deutsch Wikipedia
Astatwasserstoff — Halogenwasserstoffe sind chemische Verbindungen, die aus den entsprechenden Halogenen mit Wasserstoff gebildet werden. Die allgemeine Summenformel lautet HX, wobei X für das Halogen steht. Ihre wässrigen Lösungen nennt man… … Deutsch Wikipedia
Halogenwasserstoff — Halogenwasserstoffe sind chemische Verbindungen, die aus den entsprechenden Halogenen mit Wasserstoff gebildet werden. Die allgemeine Summenformel lautet HX, wobei X für das Halogen steht. Ihre wässrigen Lösungen nennt man… … Deutsch Wikipedia
Halogenwasserstoffsäure — Halogenwasserstoffe sind chemische Verbindungen, die aus den entsprechenden Halogenen mit Wasserstoff gebildet werden. Die allgemeine Summenformel lautet HX, wobei X für das Halogen steht. Ihre wässrigen Lösungen nennt man… … Deutsch Wikipedia
Halogenwasserstoffverbindungen — Halogenwasserstoffe sind chemische Verbindungen, die aus den entsprechenden Halogenen mit Wasserstoff gebildet werden. Die allgemeine Summenformel lautet HX, wobei X für das Halogen steht. Ihre wässrigen Lösungen nennt man… … Deutsch Wikipedia
Bleitiegeltest — Fluoride sind die Salze der Fluorwasserstoffsäure (HF), die auch als Flusssäure bekannt ist. Sie enthalten in ihrem Ionengitter als negative Gitterbausteine (Anionen) Fluorid Ionen (F−). Daneben werden auch kovalente, nicht ionische Verbindungen… … Deutsch Wikipedia