- Alundum
-
Kristallstruktur 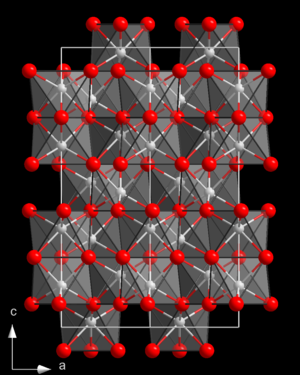
Allgemeines Name Aluminiumoxid Andere Namen - Korund (Mineral)
- Tonerde
Verhältnisformel Al2O3 CAS-Nummer 1344-28-1 Kurzbeschreibung weißes, geruchloses Pulver Eigenschaften Molare Masse 101,96 g·mol−1 Aggregatzustand fest
Dichte Schmelzpunkt Siedepunkt 2980 ± 60 °C[1]
Löslichkeit unlöslich in Wasser, schwer löslich in Säuren und Basen[1]
Sicherheitshinweise Gefahrstoffkennzeichnung [1] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: 22 MAK 1,5 mg/m3 als Feinstaub[2]
LD50 > 5000 mg·kg−1 (Ratte, oral) [1]
Thermodynamische Eigenschaften ΔHf0 −1676 kJ·mol−1[3]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Aluminiumoxid ist die Sauerstoffverbindung des chemischen Elements Aluminium. Im technischen Bereich wird Aluminiumoxid als Elektrokorund oder kurz als ELK bezeichnet.
Inhaltsverzeichnis
Modifikationen
Die wichtigsten Modifikationen des Aluminiumoxides sind:
- das kubische γ-Al2O3 (Tonerde, Ausgangsstoff zur Keramik- und Aluminiumherstellung)
- das rhomboedrische (trigonale) α-Al2O3 (bekannt als Mineral Korund, Saphir oder – bei Chromdotierung – Rubin, als Schleifmittel und Aluminiumoxid-Keramik)
- ebenso ist noch die β-Tonerde (β-Al2O3) bekannt, hierbei handelt es sich um einen historischen Irrtum. Dabei handelt es sich um die Verbindung von Na2O und Al2O3 zu Na2Al22O34 (Na2O*11Al2O3), bekannt auch unter dem Mineralnamen Diaoyudaoit[4]
Gewinnung und Darstellung
Aus Bauxit wird Aluminiumhydroxid (ATH) durch Aufschließen in Natronlauge gewonnen (Bayer-Verfahren). Durch Entziehen des Wassers, z. B. durch Brennen, Sintern oder Kalzinieren erhält man Aluminiumoxid.
Die Darstellung von Aluminiumoxid kann auch durch vorsichtiges Dehydrieren von Gibbsit (Hydrargillit) oder Böhmit erfolgen.
Aluminiumoxid entsteht zudem bei der Verbrennung von Aluminiumpulver mit Ammoniumperchlorat in Feststoffraketen.
Das reine Metall Aluminium weist nach Lagerung an Luft eine dünne spontane Aluminiumoxidschicht (Selbstpassivierung) auf, die es vor Korrosion schützt. Mittels einer elektrolytisch aufgebrachten Aluminiumoxidschicht werden durch Eloxieren die Aluminiumoberflächen von Gebrauchsgegenständen mit einer extrem harten (etwa Mohs-Härte 9) und korrosionsbeständigen Schutzschicht versehen. Zur Fertigung von Elektrolytkondensatoren verwendet man diese eloxierten Aluminiumsorten.
Eigenschaften
Das γ-Al2O3 ist ein hygroskopisches, weißes, lockeres Pulver, das nicht in Wasser, dafür in starken Säuren und Basen löslich ist.
Bereits ab 800 °C geht das γ-Al2O3 in das in Säuren wie Basen im allgemeinen unlösliche α-Al2O3 über.
Mit verschiedenen Metalloxiden bildet Aluminiumoxid Aluminate.
γ-Al2O3 ist ein poröses Material, dessen Oberflächenstruktur stark von dem Herstellungsprozess, beziehungsweise dessen Temperatur, beeinflusst werden kann. In der Chromatographie wird es als Adsorbens verwendet.
Al2O3 ist ein amphoteres Salz. D.h.: Es kann als Säure (in Verbindung mit einer Base) oder als Base (in Verbindung mit einer Säure) reagieren.
Verwendung
Hybridschaltung auf einem Aluminiumoxidkeramik-Substrat - ↑ a b c d e f SDL Merck. 20. Feb. 2007
- ↑ Eintrag zu Aluminiumoxid in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 23.12.2007 (JavaScript erforderlich)
- ↑ PAETEC Formelsammlung Ausgabe 2003, Seite 116
- ↑ http://www.webmineral.com/data/Diaoyudaoite.shtml
Das α-Al2O3 hat eine Mohs'sche Härte von 9 bis 9,5 und wird unter anderem zu Lagersteinen von Messinstrumenten und Uhren, sowie zu Schleifmitteln verarbeitet. Basis dafür ist häufig das als Nebenprodukt der Aluminothermie anfallende Alundum.
Kalzinierte Aluminiumoxide werden in der Keramik (z. B. in Zündkerzen, Waschbecken, Hotelgeschirr, schusssicherer Bekleidung) oder im weitesten Sinn als Poliermittel (z.B. in Glaskeramikreinigern, Autopflegemitteln, Bremsbelägen, Zahnpasten) verwendet. Weiterhin dient gesintertes α-Al2O3 (Sinterkorund) als feuerfestes Material in Ofenauskleidungen oder Laborgeräten.
Mit Verunreinigungen durch geringe Mengen an Cr2O3 beziehungsweise TiO2 bildet der Korund die Edelsteine Rubin (Uhrensteine, Ziehsteine, Rubinlaser) und Saphir.
Mit Ti2O3 dotierte Al2O3-Einkristalle bilden das Herzstück des Titan:Saphir-Lasers.
γ-Al2O3 dient als Adsorbens und als Katalysatorträger, sowie als Katalysator selbst.
In der Elektrotechnik wird Aluminiumoxid-Keramik wegen ihres geringen Dielektrischen Verlustfaktors als Dielektrikum eingesetzt. Haupteinsatzbereich ist dabei die Realisierung von Streifenleitungen und Kondensatoren in der Hochfrequenztechnik. Aluminiumoxid-Keramikplatten dienen auch als Substrat für die Dickschichttechnik und für Platin-Temperaturmesswiderstände (siehe PT100).
Hochreine, großkristalline und daher transparente Aluminiumoxid-Keramik dient der Herstellung von Brennerrohren von Hochdruck-Gasentladungslampen (Natriumdampflampen, Halogen-Metalldampflampen). Früher verwendete man es auch als Ultraviolett-transparentes Fenstermaterial für EPROMs.
Neueste Sinterverfahren machen es möglich, Aluminiumoxid zur Herstellung extrem fester und bruchsicherer Gläser einzusetzen, z. B. bei Armbanduhrengläsern (Nature, Vol. 430, S. 761, 2004).
In letzter Zeit werden Al2O3 Keramiken auch in Panzerungen von Fahrzeugen verwendet. Die Keramikkacheln werden dabei auf ein Aramid- bzw. Dyneema-Gewebe geklebt. Diese Art der Panzerung erreicht, bei einem gleichen Flächengewicht die doppelte Schutzwirkung von Panzerstahl. Die Keramik fragmentiert das Geschoss, die Aramid-Fasern fangen anschließend die Bruchstücke auf.
Al2O3 wird mit der Bezeichnung Elektrokorund (ELK) in den Handel als Edelkorund, Halbedelkorund und Normalkorund gebracht. In einem elektrischen Ofen wird es bei etwa 2.000 °C hergestellt. Der dabei entstehende Schmelzkuchen wird zerschlagen und nach in der DIN festgelegten Körnungen abgesiebt. Edelkorund wird in der Technik als Schleifmittel bei Herstellung von Schleifscheiben verwendet. Es wird auch als Strahlmittel und als Polierpulver verwendet.
Quellen
Siehe auch
Wikimedia Foundation.

