- Levosimendan
-
Strukturformel 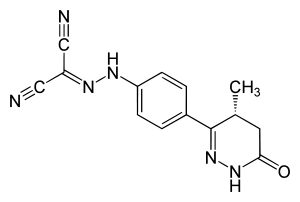
Allgemeines Freiname Levosimendan Andere Namen (''R'')-2-[[4-[4-Methyl-6-oxo-4,5-dihydro-1H- pyridazin-3-yl]phenyl]hydrazinyliden]propandinitril (IUPAC)
Summenformel C14H12N6O CAS-Nummer 141505-33-1 PubChem 3033825 ATC-Code C01CX08
DrugBank DB00922 Arzneistoffangaben Wirkstoffklasse Calcium-Sensitizer
Eigenschaften Molare Masse 280,28 g·mol−1 Sicherheitshinweise Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln EU-Gefahrstoffkennzeichnung [1] Keine Einstufung verfügbarR- und S-Sätze R: siehe oben S: siehe oben Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Levosimendan (Handelsname Simdax®; Orion Oyj) ist ein Arzneistoff aus der Gruppe der Calcium-Sensitizer, der in der Kurzzeitbehandlung der akut dekompensierten, schweren chronischen Herzinsuffizienz eingesetzt wird.
Inhaltsverzeichnis
Klinische Angaben
Anwendungsgebiete (Indikationen)
Levosimendan ist indiziert zur Kurzzeitbehandlung der akut dekompensierten, schweren chronischen Herzinsuffizienz (englisch: acutely decompensated severe chronic heart failure, ADHF) in Situationen, in denen eine konventionelle Therapie mit intravenösen Diuretika nicht ausreichend ist und eine Therapie mit inotrop wirkenden Substanzen geeignet erscheint[2].
Dosierung, Art und Dauer der Anwendung
Levosimendan ist ein Infusionslösungskonzentrat, das vor der Applikation verdünnt werden muss. Es dient nur zur Anwendung im Krankenhaus und setzt das Vorhandensein adäquater Überwachungseinrichtungen sowie Erfahrung in der Therapie mit Inotropika voraus. Die Dosis und die Behandlungsdauer sind individuell, entsprechend dem klinischen Zustand des Patienten und seinem Ansprechen auf die Behandlung, anzupassen.
Gegenanzeigen (Kontraindikationen)
Levosimendan darf nicht angewendet werden bei:
- schwerer Hypotonie (niedriger Blutdruck)
- Herzrasen (Tachykardie)
- signifikanten mechanischen Behinderungen, die die ventrikuläre Füllung, den ventrikulären Ausstrom oder beides beeinflussen (z. B. Aortenstenose)
- stark beeinträchtigter Leber- oder Nierenfunktion
- Torsade de pointes
Unerwünschte Wirkungen (Nebenwirkungen)
Als häufigste Nebenwirkungen wurden abnormal schneller Herzschlag, Blutdruckabfall und Kopfschmerzen beobachtet. Häufig kamen auch Schlaflosigkeit, Schwindel, Magen-Darm-Störungen (Übelkeit, Erbrechen, Verstopfung, Durchfall) und erniedrigte Kalium- und Hämoglobinwerte vor.
Pharmakologische Eigenschaften
Levosimendan steigert die Pumpkraft des Herzens (positiv inotrope Wirkung) und erweitert die Blutgefäße (vasodilatorische Wirkung). Die Durchblutung des Herzmuskels wird verbessert, ohne dass mehr Sauerstoff verbraucht wird.
Wirkungsmechanismus (Pharmakodynamik)
Levosimendan erhöht die Calciumsensitivität der kontraktilen Proteine, welche durch eine Bindung an das kardiale Troponin C hervorgerufen wird. Somit erhöht es die Kontraktilität (positiv inotrope Wirkung), aber beeinträchtigt nicht die ventrikuläre Entspannung, was darauf zurückzuführen ist das der transmembrane Calciumstrom nicht über pharmakologische relevante Konzentrationen hinaus erhöht wird. Zusätzlich öffnet Levosimendan Adenosintriphosphat(ATP)-sensitive Kaliumkanäle in der glatten Gefäßmuskulatur, wodurch der Gefäßwiderstand in den Koronararterien und in den systemischen (arteriellen und venösen) Gefäßen herabgesetzt wird (vasodilatorische Wirkung). Die Vor- und Nachlast des Herzens werden reduziert.
Levosimendan gehört somit zur Gruppe der Inodilatoren.
Pharmakokinetik
Levosimendan wird nahezu vollständig in der Leber metabolisiert, 54 % der Dosis werden über die Nieren und 44 % über die Fäzes ausgeschieden. Die Halbwertszeit beträgt circa 1 Stunde. Die nach Absetzen von Levosimendan noch etwa 7 bis 9 Tage anhaltende hämodynamische Wirkung ist auf die Metaboliten (OR-1855 und OR-1896) zurückzuführen, die Halbwertszeiten von 70 bis 80 Stunden aufweisen.
Sonstige Informationen
Levosimendan wurde 2000 in Schweden als weltweit erstem Land zugelassen, 2001 folgte die Zulassung in anderen europäischen Ländern. Levosimendan wurde von der finnischen Firma Orion entwickelt.
Siehe auch
Einzelnachweise
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Schwedische Fachinformation Simdax, Stand Juli 2009.

Bitte den Hinweis zu Gesundheitsthemen beachten! Kategorien:- ATC-C01
- Arzneistoff
- Nitril
- Hydrazin
- Tetrahydroazin
- Aromat
Wikimedia Foundation.
