- Rubidiumnitrat
-
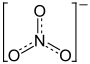
Strukturformel 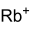
Kristallsystem hexagonal
Allgemeines Name Rubidiumnitrat Summenformel RbNO3 CAS-Nummer 13126-12-0 PubChem 25731 Kurzbeschreibung weißer Feststoff[1]
Eigenschaften Molare Masse 147,47 g·mol−1 Aggregatzustand fest
Dichte 3,11 g·cm−3[1]
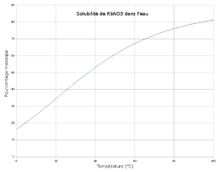
Schmelzpunkt Löslichkeit löslich in Wasser: 442,8 g·l−1 (16 °C)[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [2] 

Gefahr
H- und P-Sätze H: 272-315-319-335 EUH: keine EUH-Sätze P: 220-261-305+351+338 [2] EU-Gefahrstoffkennzeichnung [1] 

Reizend Brand-
fördernd(Xi) (O) R- und S-Sätze R: 36/37/38-8 S: 17-26-37/39 LD50 4625 mg·kg−1 (oral, Ratte)[3]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Rubidiumnitrat ist das Rubidiumsalz der Salpetersäure.
Inhaltsverzeichnis
Eigenschaften
Rubidiumnitrat bildet farblose, stark hygroskopische trigonale Kristalle, die in der Raumgruppe P31m mit den Gitterparametern a = 1047 pm und c = 745 pm sowie vier Formeleinheiten pro Elementarzelle kristallisieren, und ist gut wasserlöslich. Der Brechungsindex der Kristalle beträgt nD = 1,524.[4] Es existieren zwei weitere Modifikationen des Rubidiumnitrats, die Umwandlungstemperaturen liegen bei 161,4 °C und 219 °C.[5] Es weist eine rotviolette Flammenfärbung auf. Es ist ein starkes Oxidationsmittel und zersetzt sich beim Erhitzen zu Rubidiumnitrit und Sauerstoff:
Wenn man Rubidiumnitrat mit Salpetersäure behandelt, bilden sich die sauren Nitrate RbH(NO3)2 (Schmelzpunkt 62 °C) und RbH2(NO3)3 (Schmelzpunkt 39 - 46 °C).[5]
Darstellung (Herstellung)
Rubidiumnitrat kann durch Salzbildungsreaktion mit Salpetersäure aus Rubidiumhydroxid oder auch aus elementarem Rubidium hergestellt werden:
Verwendung
Rubidiumnitrat wird als Bestandteil von infrarot-emittierenden Leuchtmitteln zusammen mit anderen Alkalinitraten als Oxidationsmittel eingesetzt.[6]
Einzelnachweise
- ↑ a b c d e Datenblatt Rubidiumnitrat bei Acros, abgerufen am 20. Februar 2010..
- ↑ a b Datenblatt Rubidium nitrate bei Sigma-Aldrich, abgerufen am 22. April 2011.
- ↑ Safety (MSDS) data for Rubidium nitrate.
- ↑ Jean D'Ans, Ellen Lax: Taschenbuch für Chemiker und Physiker. 3. Elemente, anorganische Verbindungen und Materialien, Minerale, Band 3. 4. Auflage, Springer, 1997, ISBN 978-3-5406-0035-0, S. 690 (Eingeschränkte Vorschau in der Google Buchsuche).
- ↑ a b R. Abegg, F. Auerbach: "Handbuch der anorganischen Chemie". Verlag S. Hirzel, Bd. 2, 1908. S. 435.Volltext
- ↑ Komprimierbare Infrarot-Beleuchtungszusammensetzungen.
Wikimedia Foundation.