- 7-Amino-4-hydroxynaphthalin-2-sulfonsäure
-
Strukturformel 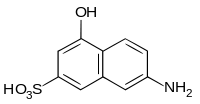
Allgemeines Name 7-Amino-4-hydroxynaphthalin-2-sulfonsäure Andere Namen - I-Säure
- J-Säure
- 7-Amino-4-hydroxy-2-naphthalinsulfonsäure
- Aminonaphtholsulfonsäure J
- Iso-γ-Säure
Summenformel C10H9NO4S CAS-Nummer 87-02-5 PubChem 6868 Kurzbeschreibung beiges Pulver[1]
Eigenschaften Molare Masse 239,25 g·mol−1 Aggregatzustand fest
Schmelzpunkt 180 - 200 °C (Zersetzung)[2]
Löslichkeit schlecht löslich in Wasser: 0,5 g·l−1 (20 °C)[2]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [1] 
Gefahr
H- und P-Sätze H: 314 EUH: keine EUH-Sätze P: 280-305+351+338-310 [1] EU-Gefahrstoffkennzeichnung [3] 
Ätzend (C) R- und S-Sätze R: 34 S: 26-27-36/37/39 LD50 > 5000 mg·kg−1 (Ratte, oral)[2]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. 7-Amino-4-hydroxy-2-naphthalinsulfonsäure ist eine der Aminohydroxynaphthalinsulfonsäuren, die als industrielle Zwischenprodukte zur Synthese von organischen, wasserlöslichen Farbstoffen wichtig sind.
Sie hat verschiedene Trivialnamen, beispielsweise I-Säure (kurz für Iso-γ-Säure) oder J-Säure (nach Paul Julius (1862−1931), Direktor der BASF AG[4]) und zählt damit zu den so genannten Buchstabensäuren.
Gewinnung und Darstellung
7-Amino-4-hydroxy-2-naphthalinsulfonsäure kann durch alkalische Hydrolyse von 2-Aminonaphthalin-5,7-disulfonsäure hergestellt werden.[2]
Verwendung
7-Amino-4-hydroxy-2-naphthalinsulfonsäure ist eine viel verwendete Kupplungskomponente zur Herstellung von Azofarbstoffen.[2] Sie ist wichtig zur Herstellung von scharlach-roten (Monoazo-) und rot-braunen (Bisazo-) Farbstoffen.
Einzelnachweise
- ↑ a b c Datenblatt 7-Amino-4-hydroxy-2-naphthalenesulfonic acid bei Sigma-Aldrich, abgerufen am 18. März 2011.
- ↑ a b c d e Toxikologische Bewertung von I-Säure (BG Chemie)
- ↑ Eintrag zu 7-Amino-4-hydroxynaphthalin-2-sulfonsäure in der GESTIS-Stoffdatenbank des IFA, abgerufen am 12. September 2010 (JavaScript erforderlich)
- ↑ Louis Fieser, Mary Fieser: Organische Chemie, Verlag Chemie Weinheim, 2. Auflage, 1972, S. 1100, ISBN 3-527-25075-1.
Wikimedia Foundation.
