- Chrom(III)-sulfat
-
Strukturformel 
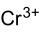
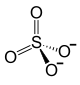
![\mathrm{ \ \!\ \Biggr]_3}](8/8189284fa3241fedf895b753c24db69c.png)
Allgemeines Name Chrom(III)-sulfat Andere Namen Chromsulfat
Summenformel - Cr2(SO4)3 (wasserfrei)
- Cr2(SO4)3 · x H2O (Hydrate)
CAS-Nummer - 10101-53-8 (wasserfrei)
- 15244-38-9 (Monohydrat)
- 10031-37-5 (Pentahydrat)
Kurzbeschreibung rotbrauner Feststoff (wasserfrei)[1], grüner oder violetter Feststoff (Hydrate)[2]
Eigenschaften Molare Masse 392,16 g·mol−1 (wasserfrei)
716,45 g·mol−1 (Dodecahydrat)Aggregatzustand fest
Dichte 3,01 g·cm−3 (Anhydrat bei 20 °C )[3]
Schmelzpunkt Löslichkeit schlecht in Wasser[3]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [5] 
H- und P-Sätze H: 302-332-315-317-319 EUH: keine EUH-Sätze P: 261-280-305+351+338-302+352-501 [5] EU-Gefahrstoffkennzeichnung [5] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 20/22-36/38-43 S: 9-24-26-37 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Chrom(III)-sulfat (Cr2(SO4)3) ist ein Salz der Schwefelsäure.
Inhaltsverzeichnis
Darstellung
Chrom(III)-sulfat kann durch die Reduktion von Dichromaten dargestellt werden:
Durch Reaktion von Kaliumdichromat, Schwefelsäure und Schwefelwasserstoff kann Chrom(III)-sulfat hergestellt werden. Als Nebenprodukte entstehen Kaliumsulfat und Wasser:
Alternativ ist zum Beispiel auch der Einsatz von Ethanol statt Schwefelwasserstoff möglich, wobei – neben dem Chrom(III)-sulfat – Kaliumsulfat, Essigsäure und Wasser entstehen:
Über diese Reaktionen erhält man allerdings kristallwasserhaltiges Chrom(III)-sulfat. Das Anhydrat lässt sich durch Entfernen des Kristallwassers bei 280 °C im CO2-Strom darstellen.[6]
Eigenschaften
Wasserfrei bildet Chrom(III)-sulfat rot-braune, hexagonale Kristalle;[1] mit Kristallwasser als Pentahydrat (Cr2(SO4)3 · 5 H2O) ist es dunkelgrün. Das Dodecahydrat und das Octadecahydrat sind hingegen lila bis violett.[2]
Absolut wasserfreies Chrom(III)-sulfat ist in Wasser unlöslich[6], die kristallwasserhaltigen Formen sind hingegen wasserlöslich.
Verwendung
Chrom(III)-sulfat wird als Textilbeize oder zur Gerbung von Leder verwendet. Es wird zudem als Ausgangsstoff für andere Chromverbindungen benutzt.[3][2]
Einzelnachweise
- ↑ a b SLAC: PHYSICAL CONSTANTS OF INORGANIC COMPOUNDS.
- ↑ a b c Jürgen Falbe, Manfred Regnitz (Hrsg.): RÖMPP-Lexikon Chemie 10. Auflage. Thieme-Verlag, Stuttgart 1996, ISBN 3-13-734610-X.
- ↑ a b c Eintrag zu Chrom(III)-sulfat in der GESTIS-Stoffdatenbank des IFA (JavaScript erforderlich).
- ↑ jtbaker.com - Chromium Sulfate.
- ↑ a b c Datenblatt Chrom(III)-sulfat bei AlfaAesar, abgerufen am 15. Dezember 2010 (JavaScript erforderlich).
- ↑ a b Gmelins Handbuch der anorganischen Chemie - Nr. 52 Chrom, Die Verbindungen (ohne Komplexbindungen mit neutralen Liganden), 8. Auflage Berlin, 1962.
Kategorien:- Gesundheitsschädlicher Stoff
- Sensibilisierender Stoff
- Sulfat
- Chromverbindung
Wikimedia Foundation.





