- Cobalt(II)-sulfid
-
Kristallstruktur 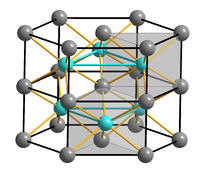
__ Co2+ __ S2- Allgemeines Name Cobalt(II)-sulfid Andere Namen - Kobalt(II)-sulfid
- Cobaltmonosulfid
- Kobaltmonosulfid
Verhältnisformel CoS CAS-Nummer 1317-42-6 PubChem 14832 Kurzbeschreibung grauer oder schwarzer Feststoff
Eigenschaften Molare Masse 91,00 g·mol−1 Aggregatzustand fest
Dichte 5,45 g·cm-3[1]
Schmelzpunkt > 1116 °C[1]
Löslichkeit - praktisch unlöslich in Wasser (3,8 mg·l−1 bei 18 °C)[1]
- löslich in Salzsäure
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [2] 

Achtung
H- und P-Sätze H: 317-410 EUH: keine EUH-Sätze P: 261-280-302+352-321-363-501 [1] EU-Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 

Reizend Umwelt-
gefährlich(Xi) (N) R- und S-Sätze R: 43-50/53 S: (2)-24-37-60-61 LD50 > 5000 mg·kg−1 (oral Ratte)[1]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Cobalt(II)-sulfid ist eine chemische Verbindung aus der Gruppe der Cobaltverbindungen und Sulfide.
Inhaltsverzeichnis
Vorkommen
Cobalt(II)-sulfid kommt natürlich in Form des Minerals Jaipurit vor.[3]
Gewinnung und Darstellung
α-Cobalt(II)-sulfid kann durch Reaktion von Cobalt(III)-nitrat mit Schwefelwasserstoff erzeugt werden.[4]
β-Cobalt(II)-sulfid kann durch direkte Synthese aus den Elementen gewonnen werden.[4]
Es kann auch durch Fällung einer mit Essigsäure versetzten Cobalt(II)-chlorid-Lösung mit Schwefelwasserstoff dargestellt werden.
Eigenschaften
Cobalt(II)-sulfid ist ein nicht brennbarer Feststoff, welcher unlöslich in Wasser ist.[1] Er kommt in zwei verschiedenen Kristallformen vor. α-Cobalt(II)-sulfid ist ein schwarzes Pulver, welches in Salzsäure löslich ist und an Luft Co(OH)S bildet. β-Cobalt(II)-sulfid ist ein graues Pulver. Es ist in Säuren löslich und wandelt sich durch anhaltende Temperung bei 200 °C in eine komplizierter gebaute Modifikation um. Es besitzt eine Kristallstruktur des NiAs-Typ (Raumgruppe C6mc, a = 3,367, c = 5,160 Å) und ist nicht homogen stöchiometrisch aufgebaut, so dass sich eine Zusammensetzung von CoS1,04 bis CoS1,13 ergibt.[4]
Verwendung
Cobalt(II)-sulfid wird als Katalysator für die Druckhydrierung organischer Verbindungen verwendet.[4]
Einzelnachweise
- ↑ a b c d e f Eintrag zu CAS-Nr. 1317-42-6 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. November 2010 (JavaScript erforderlich)
- ↑ a b Eintrag zu CAS-Nr. 1317-42-6 im European chemical Substances Information System ESIS (ergänzender Eintrag)
- ↑ Jaipurite (Mindat)
- ↑ a b c d Brauer,Georg;Handbuch der präparativen anorganischen Chemie, S.1667;ISBN 3-432-87813-3
Wikimedia Foundation.


